
下列表述中正确的是
A.任何能使熵值增大的过程都能自发进行
B.△H<0,△S>0的化学反应一定能自发进行
C.已知热化学方程式2SO2(g)+O2(g) 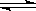 2SO3(g) △H=-QkJ·mol-1(Q>0),则将2mol SO2(g) 和1mol O2(g) 置于一密闭容器中充分反应后放出Q kJ的热量
2SO3(g) △H=-QkJ·mol-1(Q>0),则将2mol SO2(g) 和1mol O2(g) 置于一密闭容器中充分反应后放出Q kJ的热量
D.稀溶液中1mol NaOH分别和1mol CH3COOH、1molHNO3反应,两者放出的热量一样多
B
【解析】
试题分析:A、反应能否自发进行不单取决于熵的变化,还受反应热的影响,△G=△H-T·△S,错误;B、从△G=△H-T·△S 中可以看出,△H<0,△S>0的化学反应中,△G<0,一定能自发进行,正确;C、△H=-QkJ·mol-1Q的具体含义是:当2mol 的二氧化硫与1mol 的氧气完全反应生成2mol 的三氧化硫时,放出的热量为QkJ ,但这是一个可逆反应,不可能完全反应,因此放出的热量小于Q kJ,错误;D、1mol NaOH分别和1mol CH3COOH反应时,放出的热量其中有一小部分用于醋酸的电离,因此放出的热量总体上来说就比硝酸与氢氧化钠的反应少一点,错误。
考点:考查反应热以及反应进行的方向的判断。


科目:高中化学 来源:2015届湖南省益阳市高二下学期第一次月考化学试卷(解析版) 题型:选择题
下列除去杂质(括号内物质为少量杂质)的方法中,正确的是
A.乙烷(乙烯):光照条件下通入Cl2,气液分离
B.乙酸乙酯(乙酸):用饱和碳酸钠溶液洗涤,分液
C.CO2(SO2):气体通过盛氢氧化钠溶液的洗气瓶
D.乙醇(乙酸):加足量浓硫酸,蒸馏
查看答案和解析>>
科目:高中化学 来源:2015届湖北省高二上学期期末考试化学试卷(解析版) 题型:选择题
常温下,将100 mL 的0.02 mol·L-1的Ba(OH)2溶液和100 mL 的0.02 mol·L-1的NaHSO4
溶液混合,若忽略溶液体积变化,则混合后的溶液
A.pH=2
B.pH=12
C.由水电离产生的c(H+)=1.0×10-2 mol·L-1
D.溶质的物质的量浓度为0.02 mol·L-1
查看答案和解析>>
科目:高中化学 来源:2015届湖北省荆门市高二上学期期末质量检测化学试卷(解析版) 题型:选择题
已知CuSO4溶液分别与Na2CO3溶液、Na2S溶液的反应情况如下:
(1)CuSO4+Na2CO3:Cu2++CO32-+H2O=Cu(OH)2↓+CO2↑
(2)CuSO4+Na2S: Cu2++S2-=CuS↓
下列几种物质的溶解度大小的比较中,正确的是
A.CuS<Cu(OH)2<CuCO3 B.CuCO3<Cu(OH)2<CuS
C.CuS<CuCO3<Cu(OH)2 D.Cu(OH)2<CuCO3<CuS
查看答案和解析>>
科目:高中化学 来源:2015届湖北省荆门市高二上学期期末质量检测化学试卷(解析版) 题型:选择题
在蒸发皿中加热蒸干并灼烧下列物质的溶液,可以得到该物质的是
A.硫酸镁 B.碳酸氢钠 C.氯化铝 D.盐酸溶液
查看答案和解析>>
科目:高中化学 来源:2015届湖北省荆门市高二上学期期末考试化学试卷(解析版) 题型:选择题
下列有关实验的叙述中,合理的是
A.用pH试纸测得氯水的pH为2
B.电解氯化镁溶液在阴极析出金属镁。
C.向Na2CO3与NaOH的混合溶液中只需加入酚酞试液,即可确认NaOH的存在
D.实验室配制氯化亚铁溶液时,可先将氯化亚铁溶解在盐酸中,再加入蒸馏水稀释,最后加入少量铁屑
查看答案和解析>>
科目:高中化学 来源:2015届湖北省荆门市高二上学期期末考试化学试卷(解析版) 题型:选择题
已知CuSO4溶液分别与Na2CO3溶液、Na2S溶液的反应情况如下:
(1)CuSO4+Na2CO3:Cu2++CO32-+H2O=Cu(OH)2↓+CO2↑
(2)CuSO4+Na2S: Cu2++S2-=CuS↓
下列几种物质的溶解度大小的比较中,正确的是
A.CuS<Cu(OH)2<CuCO3 B.CuCO3<Cu(OH)2<CuS
C.CuS<CuCO3<Cu(OH)2 D.Cu(OH)2<CuCO3<CuS
查看答案和解析>>
科目:高中化学 来源:2015届湖北省荆州市部分县市高二上学期期末考试化学试卷(解析版) 题型:选择题
依据甲、乙、丙三图回答下列问题:

(1)甲装置为__________,乙装置为__________,丙装置为__________。
(2)甲、乙装置中,锌极上分别发生__________反应、__________反应。
(3)乙装置中,Cu2+浓度__________。
查看答案和解析>>
科目:高中化学 来源:2015届湖北省三校高二上学期期末联考化学试卷(解析版) 题型:填空题
已知0.1mol/L H2SO4在水中的第一步电离是完全的,第二步电离并不完全。常温下有0.1mol/L的以下几种溶液的电离度(即已经电离的分子数占原来分子总数的百分数)如下表,回答下列问题:
①H2SO4溶液中的HSO4– | ②NaHSO4溶液中的HSO4– | ③CH3COOH | ④HCl溶液 |
10% | 29% | 1.33% | 100% |
(1)写出H2SO4在水中的电离方程式 。
(2)常温下,题设条件下的①溶液中c(H+)= 。
(3)常温下,pH相同的上述几种溶液,其物质的量浓度由大到小的顺序是(填序号) 。
(4)若将10mL题设条件下的NaHSO4溶液与0.1mol/LNaOH溶液等体积混合,则混合后溶液中离子浓度由大到小顺序为 。
(5)根据题设条件计算CH3COOH的电离常数Ka= 。若常温下,将b mol·L–1的CH3COONa液与0.01 mol·L–1的盐酸等体积混合,反应达平衡时,测得溶液的pH=7,用含b的代数式表示CH3COOH的电离常数Ka= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com