
下列关于物质应用的说法正确的是( )
A.P2O5可用于干燥Cl2和NH3
B.玻璃容器可长期盛放各种酸
C.浓氨水可检验氯气管道漏气
D.Si和SiO2都用于制造光导纤维
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列有关物质性质的说法错误的是( )
A.热稳定性:HCl>HI B.原子半径:Na>Mg
C.酸性:H2SO3>H2SO4 D.结合质子能力:S2->Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子或分子在溶液中能大量共存,且满足相应要求的是( )
| 选项 | 离子或分子 | 要求 |
| A | K+、NO | c(K+)<c(Cl-) |
| B | Fe3+、NO | 逐滴滴加盐酸立即有气体产生 |
| C | Na+、HCO | 逐滴滴加氨水立即有沉淀产生 |
| D | NH | 滴加NaOH浓溶液立刻有气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.常温常压下,33.6 L氯气与27 g铝充分反应,转移电子数为3NA
B.标准状况下,分子数为NA的CO、N2混合气体体积为22.4 L,其质量为28 g
C.50 mL 8 mol·L-1的浓盐酸与足量的MnO2加热反应,生成Cl2的分子数为0.1NA
D.标准状况下,80 g SO3中含3NA个氧原子,体积为22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,下列说法正确的是(双选)( )
A.在1 L 0.1 mol·L-1的硫化钠溶液中,阴离子总数大于0.1NA
B.1 mol O2作氧化剂时转移电子数一定为4NA
C.1 mol硫酸钾固体中阴离子所带电荷数为2NA
D.在1 L 1.0 mol·L-1 NaCl溶液中含有NA个NaCl分子
查看答案和解析>>
科目:高中化学 来源: 题型:
以下非金属氧化物与其引起的环境问题及主要来源对应正确的是( )
| 选项 | 氧化物 | 环境问题 | 主要来源 |
| A | CO | 煤气中毒 | 含碳燃料的不完全燃烧 |
| B | SO2 | 光化学烟雾 | 汽车尾气的排放 |
| C | NO2 | 温室效应 | 工厂废气的排放 |
| D | CO2 | 酸雨 | 化石燃料的燃烧 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组在课外活动中,对某一份溶液成分(已知不含其他还原性离子)进行了检测,其中三次检测结果如表所示:
| 检测序号 | 溶液中检测出的电解质溶液组合 |
| 第一次 | KCl、K2SO4、Na2CO3、NaCl |
| 第二次 | KCl、AlCl3、Na2SO4、K2CO3 |
| 第三次 | Na2SO4、KCl、K2CO3、NaCl |
则下列说法合理的是( )
A.三次检测结果都正确
B.该溶液中的阳离子无法判断
C.为了检验是否存在SO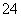 ,应先加过量稀硝酸后再滴加Ba(NO3)2溶液,观察是否有沉淀产生
,应先加过量稀硝酸后再滴加Ba(NO3)2溶液,观察是否有沉淀产生
D.为了检验是否存在CO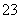 ,可以向溶液中滴加CaCl2溶液,观察是否有沉淀产生
,可以向溶液中滴加CaCl2溶液,观察是否有沉淀产生
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒容密闭容器中A(g)+3B(g)  2C(g) ΔH<0,达平衡后,将气体混合物的温度降低,下列叙述中不正确的是( )
2C(g) ΔH<0,达平衡后,将气体混合物的温度降低,下列叙述中不正确的是( )
A.混合气体密度的变化情况不可以作为判断反应是否再次达平衡的依据
B.容器中混合气体的平均相对分子质量增大
C.正反应速率和逆反应速率都变小,C的百分含量增加
D.正反应速率增大,逆反应速率减小,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,通过下列反应可以制备特种陶瓷的原料MgO:MgSO4s)+COg)MgOs)+CO2g)+SO2g) ΔH>0
该反应在恒容密闭容器中达到平衡后,若仅改变图中横坐标x的值,纵坐标y随x变化趋势合理的是 )。
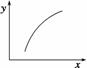
| 选项 | x | y |
| A | 反应时间 | CO2与CO的物质的量之比 |
| B | 反应温度 | 逆反应速率 |
| C | 体系压强 | 平衡常数K |
| D | MgSO4的质量 | CO的转化率 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com