
【题目】标准状况下,VL氨气溶解在1L水中(水的密度近似为lg/mL),所得溶液的密度为ρg/mL,质量分数为ω,物质浓度为c mol/L,则下列关系中不正确的是
A. ρ=![]() B. ω=
B. ω=![]() C. ω=
C. ω=![]() D.
D. ![]()
 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:
【题目】实验室中需要配制0.2 mol/L的CuSO4溶液950 mL,配制时应选用的容量瓶的规格和称取的CuSO4的质量分别是( )
A.950 mL 30.4 gB.500 mL 16 g
C.1 000 mL 32 gD.任意规格 30.4 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去SiO2中混有的少量生石灰和石灰石,有如下操作:①加水溶解 ②加水煮沸③过滤 ④加稀HCl ⑤加稀H2SO4,正确的操作顺序是
A.①③B.④③C.⑤③D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学为了探究铜与浓硫酸的反应,进行了如下实验,实验装置如图所示。

实验步骤:
①先连接如图所示的装置,检查好气密性,再加入试剂;
②加热A试管,待B试管中品红溶液退色后,熄灭酒精灯;
③将Cu丝向上抽动离开液面。
请回答下列问题:
(1)A试管中发生反应的化学方程式为____________________________________________。
(2)能够证明铜与浓硫酸反应生成气体的实验现象是_______________________________。
(3)在盛有BaCl2溶液的C试管中,除了导管口有气泡外,无其他明显现象,若将其中的溶液分成两份,分别滴加下列溶液,将产生沉淀的化学式填入表中对应的位置。
滴加的溶液 | 氯水 | 氨水 |
沉淀的化学式 | ________ | ________ |
写出其SO2表现还原性的离子反应方程式:______________________________________。
(4) 装置D的作用__________________________________________________________ 。
(5)实验完毕后,先熄灭酒精灯,由于导管E的存在,试管B中的液体不会倒吸入试管A中,其原因是_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂的一个生产工艺流程如图所示,下列叙述正确的是( )
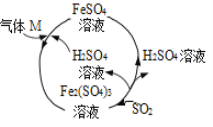
A. 该工艺流程的目的是制备 Fe2(SO4)3
B. 气体 M一定是 SO3
C. 气体 M 参加的反应是化合反应
D. SO2 参加反应时氧化剂和还原剂的物质的量之比是 1∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的镁、铜合金加入到稀硝酸中,两者恰好完全反应,假设反应过程中还原产物全是NO,向所得溶液中加入物质的量浓度为3mol·L-1 的NaOH溶液至沉淀完全,测得生成沉淀的质量比原合金的质量增加5.1g,则下列有关叙述中正确的是
A. 开始加入合金的质量可能为16.4g
B. 标准状况下产物NO的体积为22.4L
C. 生成沉淀完全时消耗NaOH溶液的体积为100mL
D. 参加反应的硝酸的物质的量为0.1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为研究生铁(含碳)与浓硫酸的反应情况及产物的性质,设计如下实验。请回答下列问题:

(1)装置b的名称______________;按如图所示装置进行实验(夹持装置及尾气处理装置未画出)。实验过程中,装置B中观察到的现象是________________;装置C中有白色沉淀生成,该沉淀是____(填化学式)。
(2)装置A中还会产生CO2气体,请写出产生CO2的化学方程式:_______________________________。
(3)为了验证装置A中产生的气体中含有CO2,应先从下列①~④中选出必要的装置(最简单)连接A装置中c处管口,从左到右的顺序为_____________________(填序号);然后再进行的操作是从a处多次鼓入N2,其目的是_____________________________。



碱石灰① 品红溶液② 高锰酸钾溶液③ 澄清石灰水④
(4)某同学通过验证实验后期装置A中产生的气体中还含有H2,理由是____________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质间可能包括多步反应,其总的离子方程式正确的是 ( )
A. 向NaClO溶液中通入过量SO2:ClO-+SO2+H2O===HClO+HSO3-
B. 向FeBr2溶液中通入少量Cl2:2Fe2++4Br-+3Cl2===2Fe3++2Br2+6Cl-
C. 向 AlCl3溶液中投入过量Na:Al3++4Na+2H2O===AlO2-+4Na++2H2↑
D. 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42- 沉淀完全:2Al3++3SO![]() +3Ba2++6OH-===2Al(OH)3↓+3BaSO4↓
+3Ba2++6OH-===2Al(OH)3↓+3BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室需要0.1 mol·L-1NaOH溶液450 mL和0.5 mol·L-1硫酸溶液500 mL。根据这两种溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是________(填序号),配制上述溶液还需用到的玻璃仪器是________(填仪器名称)。

(2)下列操作中,容量瓶所不具备的功能有________(填序号)。
A.配制一定体积准确浓度的标准溶液 B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体 D.准确稀释某一浓度的溶液
E.用来加热溶解固体溶质
(3)根据计算用托盘天平称取NaOH的质量为________g。在实验中其他操作均正确。若NaOH溶液在转移至容量瓶时未经冷却,则所得溶液浓度________(填“大于”“等于”或“小于”)0.1 mol·L-1。
(4)根据计算得知,所需质量分数为98%、密度为1.84 g·cm-3的浓硫酸的体积为________mL(计算结果保留一位小数)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com