


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
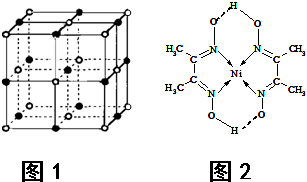 (2013?渭南二模)决定物质性质的重要因素是物质结构.请回答下列问题.
(2013?渭南二模)决定物质性质的重要因素是物质结构.请回答下列问题.| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
| 共价键 | C-C | C-N | C-S |
| 键能/kJ?mol-1 | 347 | 305 | 259 |
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ?mol-1 | 786 | 715 | 3401 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
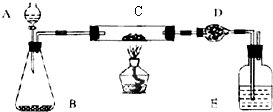
| 实 实验过程 | 实验现象 | 有关化学方程式 | ||||||||||||||||
| 在C中加入样品标本W克,D中装入药品后并称量为m1克.连接好仪器后,检查气密性 | B、E中有气泡产生 B、E中有气泡产生 |
2H2O2
2H2O2
| ||||||||||||||||
| 打开A的活塞,慢慢滴加溶液. | C中的红褐色粉末变成黑色 C中的红褐色粉末变成黑色 |
2Cu+O2
2Cu+O2
| ||||||||||||||||
| 对C进行加热.当C中药品充分反应后.关闭A的活塞.停止加热: | 无 无 |
无 无 | ||||||||||||||||
| 冷却后,称量D的质量为m2克. | 无 无 |
无 无 |
W-(m2-m1)×
| ||
| W |
W-(m2-m1)×
| ||
| W |
查看答案和解析>>
科目:高中化学 来源:2012届江苏省扬州中学高三12月练习测试化学试卷 题型:填空题
(12分)决定物质性质的重要因素是物质结构。请回答下列问题。
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
| 共价键 | C-C | C-N | C-S |
| 键能/ kJ·mol-1 | 347 | 305 | 259 |

| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
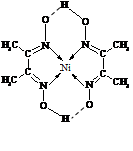
查看答案和解析>>
科目:高中化学 来源:2012届河北省高二4月月考化学试卷 题型:实验题
(Ⅰ)某校合作探究小组利用业余时间上网搜索烯类化合物与溴加成反应的有关信息,获得的有关结构与数据列表如下(以乙烯为标准)
|
烯 类 化 合 物 |
相 对 速 率 |
|
(CH3)2C=CHCH3 |
10.4 |
|
CH3CH=CH2 |
2.03 |
|
CH2=CH2 |
1.00 |
|
CH2=CHBr |
0.04 |
(1)据表中数据,总结烯类化合物加溴时,反应速率与碳碳双键上取代基的种类、个数间的关系:___________________________ ______ 。
(2)下列化合物与氯化氢加成时,取代基对速率的影响与上述规律类似,其中反应速率最慢的是_________。
A.(CH3)2C= C (CH3)2 B.CH3CH=CHCH3 C.CH2=CH2 D.CH2=CHCl
 (Ⅱ)另一合作探究小组根据所学知识归纳整理乙醇、水、苯酚、碳酸( HO—C—OH)、乙酸分子中羟基上氢原子的活泼性。
O
(Ⅱ)另一合作探究小组根据所学知识归纳整理乙醇、水、苯酚、碳酸( HO—C—OH)、乙酸分子中羟基上氢原子的活泼性。
O
(1)甲同学将一些化学实验收集整理如下:
A.金属钠分别与水和乙醇反应 B.苯酚、二氧化碳、乙酸分别与氢氧化钠溶液反应
C.向二氧化碳水溶液、乙酸溶液中分别滴加紫色石蕊试液
D.将鸡蛋壳破碎后加入到醋酸溶液中 E.向苯酚溶液中滴加FeCl3溶液
F.向苯酚钠溶液中分别通入二氧化碳和滴加盐酸
其中能说明水比乙醇强的是 (填字母,下同),乙酸比碳酸强的是 。
(2)乙同学与其他同学合作,设计了一个简单的一次性完成的实验装置来验证乙酸、碳酸和苯酚溶液的酸性强弱,以说明其羟基上氢原子的活泼性顺序。根据下列实验装置图回答有关问题。
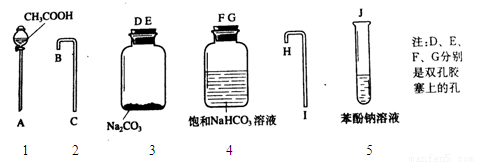
① A对应的仪器名称是 ;
② 各仪器的连接顺序是(填数字,仪器可重复使用) ;
③ 饱和NaHCO3溶液作用是 ;
④ 实验过程中观察到的现象有 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com