
| 序号 | 实验操作 | 实验现象 | 实验结论 |
| ① | 将镁条投入5mL蒸馏水 | 微量气泡 | Mg与蒸馏水缓慢反应 |
| ② | 将镁条投入5mL饱和NaHCO3溶液中 | 镁表面出现大量气泡 | Mg与NaHCO3溶液剧烈反应 |
| ③ | 将镁条投入5mLNaOH溶液中 | 现象不明显 | Mg与NaOH溶液较难反应 |
| 实验步骤 | 想象和结论 |
| 大试管中加入擦去氧化膜的镁条 |
分析 (1)配制饱和溶液,只要溶液中有没有溶解的固体NaHCO3,溶液饱和;饱和NaHCO3溶液pH=8.4,是因为HCO3-的水解程度大于其电离程度;
(2)①据实验现象为微量气泡判断实验结论;
②据Mg与NaHCO3溶液剧烈反应判断实验现象;
(3)Mg与NaHCO3溶液反应,可能生成二氧化碳和氢气,据此分析.
解答 解:(1)配制饱和NaHCO3溶液,在烧杯中加入足量的碳酸氢钠固体,加入适量蒸馏水,加热使之溶解,冷却后取上层清液即可;饱和NaHCO3溶液pH=8.4,是因为HCO3-的水解大于其电离,其水解的离子方程式为:HCO3-+H2O?H2CO3+OH-,
故答案为:在烧杯中加入足量的碳酸氢钠固体,加入适量蒸馏水,加热使之溶解,冷却后取上层清液即可;HCO3-+H2O?H2CO3+OH-;
(2)①实验现象为微量气泡,说明Mg与蒸馏水缓慢反应,故答案为:Mg与蒸馏水缓慢反应;
②Mg与NaHCO3溶液剧烈反应,可知镁表面出现大量气泡,故答案为:镁表面出现大量气泡;
(3)Mg与NaHCO3溶液反应,可能生成二氧化碳和氢气,所以假设一:只有CO2时,假设二:只有H2;假设三:两种气体都有,检验二氧化碳气体的存在,可以用湿润的红色石蕊试纸检验,故答案为:H2;H2和CO2;
| 实验步骤 | 想象和结论 |
| 加入碳酸氢钠饱和溶液,用湿润的红色石蕊试纸在锥形瓶口检验 | 若试纸变红,气体中有CO2 若试纸不变红,气体中无CO2 |
点评 本题考查了饱和溶液的配制、水解离子方程式书写、实验现象的分析判断、气体的检验,题目难度较大.


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:高中化学 来源: 题型:选择题
| A. | 将大小、形状相同的镁条和铝条与相同浓度、相同温度下的盐酸反应时,两者快慢相同 | |
| B. | 盛有相同浓度双氧水的两支试管,一支加入MnO2放在冷水中,一支直接放在冷水中,前者反应快 | |
| C. | 将浓硝酸分别放在冷暗处和强光下,发现强光下的浓硝酸分解得快 | |
| D. | 升高温度,H2O2的分解速率加快,原因是反应物分子的能量增加,活化分子百分数增大,有效碰撞次数增多 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将LiCoO2改写成为氧化物的形式为Li2O•Co2O3 | |
| B. | 该电池的电解液必须使用有机溶剂主要是由于有机溶剂有良好的导电性 | |
| C. | Li是3号元素,是最轻的金属之一,这类电池质能比高 | |
| D. | 在电池充放电时,Li+在两个电极之间往返嵌入和脱嵌.该电池的充放电反应方程式为:LiCoO2+6C$?_{放电}^{充电}$Li1-xCoO2+LixC6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
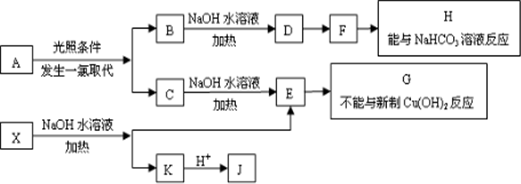
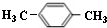 .
.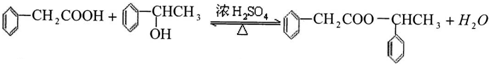 ;该反应类型是酯化反应(或取代反应).
;该反应类型是酯化反应(或取代反应).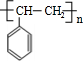 .
.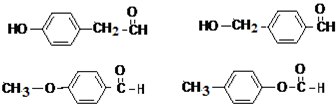 任意一种.
任意一种.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
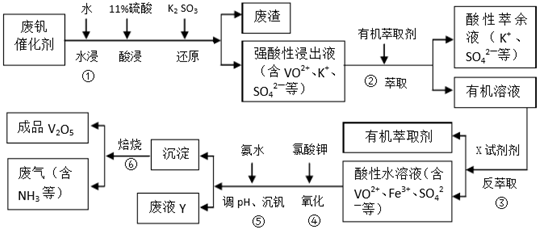
| pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
| 钒沉淀率/% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.6 | 96.4 | 93.1 | 89.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
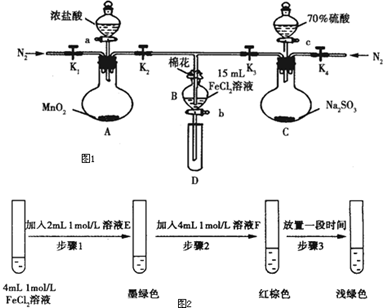
| 过程Ⅳ:B溶液中含有的离子 | 过程Ⅵ:B溶液中含有的离子 | |
| 甲 | 有Fe3+,无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+、又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+、无Fe2+ | 有Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
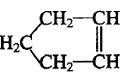 可简写为
可简写为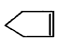 ,降冰片烯的分子结构可表示为:
,降冰片烯的分子结构可表示为: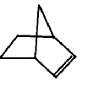
| A. | 易溶于水 | B. | 能发生氧化反应 | C. | 能发生加成反应 | D. | 能发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
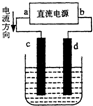
| A. | a为负极、b为正极 | B. | c电极上发生还原反应 | ||
| C. | 电解过程中,d电极质量增加 | D. | 电解过程中,氯离子浓度不变 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com