
弱电解质的电离程度可用电离度( )表示:
)表示: ,现有pH均为4的HCl和
,现有pH均为4的HCl和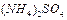 溶液,则两种溶液中H2O的电离度之比为( )
溶液,则两种溶液中H2O的电离度之比为( )
| A.1:2 | B.2:5 | C.1:106 | D.106:1 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| c(CH3COO-)?c(H+) |
| c(CH3COOH) |
| c(CH3COOH)?c(OH-) |
| c(CH3COO-) |
| Ka.c |
| Ka.c |
查看答案和解析>>
科目:高中化学 来源:2013届度黑龙江大庆实验中学高二上学期期末考试化学试卷 题型:选择题
下列关于弱电解质的说法正确的是: ( )
A.电解质越弱,则其溶液的导电能力就越差
B.同一弱电解质,浓度越大,电离程度越大
C.升高温度,弱电解质的电离程度减小
D.弱电解质的相对强弱可由相同温度下的电离常数值的大小来判断
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com