
氢化热是指一定条件下,1mol不饱和化合物加氢时放出的热量.表中是环己烯( )、环己二烯(
)、环己二烯( )和苯的氢化热数据:
)和苯的氢化热数据:
| 物质 |
|
|
|
| 氢化热(kJ/mol) | 119.7 | 232.7 | 208.4 |
根据表中数据推断正确的是( )
|
| A. | 环己二烯与H2的反应最剧烈 |
|
| B. | 环己烯、环己二烯和苯有相同的官能团 |
|
| C. | 三种化合物中环己二烯的稳定性最强 |
|
| D. | 上述条件下,1 mo |
| 反应热和焓变. | |
| 专题: | 化学反应中的能量变化. |
| 分析: | A、断裂1mol碳碳键放出热量越多反应越剧烈; B、依据环己烯、环己二烯和苯的分子结构分析判断官能团; C、物质能量越低越稳定; D、环己二烯转变为环己烯时是和氢气加成完成是放热反应,放热可以依据盖斯定律计算判断; |
| 解答: | 解:A、断裂1mol碳碳键环己烯放热为119.7KJ、环己二烯放热为116.35KJ、苯放热69.47KJ,所以环己烯氢化反应剧烈,故A错误; B、环己烯官能团为一个双键、环己二烯含两个双键、苯分子中是六个碳碳键完全等同的化学键,所以不是有相同的官能团,故B错误; C、断裂1mol碳碳键环己烯放热为119.7KJ、环己二烯放热为116.35KJ、苯放热69.47KJ,三种化合物中苯的稳定性最强,故C错误; D、①C6H10+H2→C6H12 氢化热为﹣119.7KJ/mol,②C6H8+2H2→C6H12 氢化热为﹣232.7KJ/mol;依据盖斯定律②﹣①得到:C6H8+H2→C6H10;氢化热为﹣113kJ/mol,所以1mol环己二烯转变为环己烯时放热113 kJ,故D正确; 故选D. |
| 点评: | 本题考查了反应氢化热的概念应用和物质加成反应的氢化热的大小比较,盖斯定律的应用,苯的分子结构的理解应用,关键是氢化热概念的理解应用. |


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:
A与B在容积为1 L的密闭容器中发生反应:aA(s)+bB(g) cC(g)+dD(g),t1,、t2时刻分别测得部分数据如下表:
cC(g)+dD(g),t1,、t2时刻分别测得部分数据如下表:
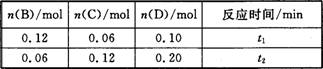
下列说法正确的是
A.0~t1时间段内,平均反应速率v(B)=0.04/t1 mol·(L·min)-1
B.若起始时n(D)=0,则t2时v(D)=0.20/t2 mol·(L·min)-1
C.升高温度,v(B)、vC)、v(D)均增大
D.b:d=6:1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学反应的速率,一定是前者大于后者的( )
|
| A. | 反应A+B |
|
| B. | 相同温度下,与同浓度盐酸反应的锌粉和铁粉产生氢气的速率 |
|
| C. | 相同温度下,颗粒大小相同的生铁分别在水和饱和食盐水中的腐蚀生锈 |
|
| D. | 一定温度下,相同氢离子浓度、相同体积的盐酸与硫酸分别与大小相同的锌片反应,产生气泡的快慢 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于乙醇的说法不正确的是( )
A.可用纤维素的水解产物制取 B. 可由乙烯通过加成反应制取
C.与乙醛互为同分异构体 D. 可以用于制取乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
下表中对应关系正确的是( )
| A | CH3CH3+Cl2CH3CH2Cl+HCl CH2=CH2+HCl→CH3CH2Cl | 均为取代反应 |
| B | 由油脂得到甘油; 由淀粉得到葡萄糖 | 均发生了水解反应 |
| C | Cl2+2Br‾═2Cl‾+Br2; Zn+Cu2+═Zn2++Cu | 均为单质被还原的置换反应 |
| D | 2Na2O2+2H2O+4NaOH+O2↑;Cl2+H2O═HCl+HClO | 均为水作还原剂的氧化还原反应 |
|
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:
碳纳米管是近年来材料科学研究的热点.为除去碳纳米管中的杂质﹣﹣碳纳米颗粒(少量碳原子的聚集体),可以将样品溶解于强酸性的K2Cr2O7溶液中充分反应,当溶液由橙色转变为墨绿色(Cr3+)即可,同时放出一种无毒的气体.以下判断正确的是( )
|
| A. | 可以用浓盐酸调节K2Cr2O7溶液的酸性 |
|
| B. | 该过程中每氧化2 mol碳纳米颗粒,转移8NA个电子 |
|
| C. | 若将该反应设计为原电池,则碳纳米颗粒应作为原电池的正极 |
|
| D. | 可以通过过滤的方法最终得到碳纳米管 |
查看答案和解析>>
科目:高中化学 来源: 题型:
焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一.某研究小组进行如下实验:
实验一 焦亚硫酸钠的制取
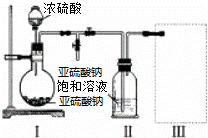
采用如图装置(实验前已除尽装置内的空气)制取Na2S2O5.装置Ⅱ中有Na2S2O5晶体析出,发生的反应为:Na2SO3+SO2═Na2S2O5
(1)装置Ⅰ中产生气体的化学方程式为 .
(2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是 .
(3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹时仪器已略去)为 (填序号)

实验二 焦亚硫酸钠的性质
Na2S2O5溶于水即生成NaHSO3.
(4)证明NaHSO3溶液中HSO3﹣的电离程度大于水解程度,可采用的实验方法是 .
a.测定溶液的pH b.加入Ba(OH)2溶液 c.加入盐酸
d.加入品红溶液 e.用蓝色石蕊试纸检测
(5)检验Na2S2O5晶体在空气中已被氧化的实验方案是 .
实验三 葡萄酒中抗氧化剂残留量的测定
(6)葡萄酒常用Na2S2O5作抗氧化剂.测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:

(已知:滴定时反应的化学方程式为SO2+I2+2H2O═H2SO4+2HI)
①按上述方案实验,消耗标准I2溶液25.00mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为 g•L﹣1.
②在上述实验过程中,若有部分HI被空气氧化,则测定结果 (填“偏高”“偏低”或“不变”).
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组有机物的混合物,只有总质量一定,无论按何比例混合,完全燃烧后生成CO2和H2O都不是恒量的是( )
A.C2H4O、C4H8O2 B.C2H4、C3H6
C.C10H8、C9H 20 D.C3H8O3、C7H8
20 D.C3H8O3、C7H8
查看答案和解析>>
科目:高中化学 来源: 题型:
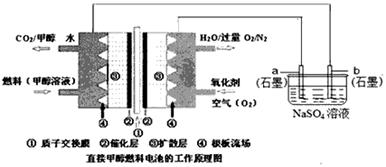
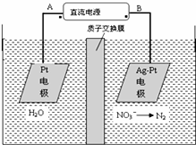 (1)化学在环境保护中趁着十分重要的作用,催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染。电化学降解NO3—的原理如图所示。
(1)化学在环境保护中趁着十分重要的作用,催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染。电化学降解NO3—的原理如图所示。
|
 ①直流电源A为 极,阳极反应式为 。
①直流电源A为 极,阳极反应式为 。 ②若电解过程中转移了2mol电子,则电源B端连接的电极产生的标况下的气体体积为 L。




|
②碱性条件下,通入甲醇的一极发生的电极反应式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com