
���Σ�3PbO��PbSO4��H2O��������������ϩ�����ȶ�����200�����Ͽ�ʼʧȥ�ᾧˮ��������ˮ���л��ܼ�����200.0tǦ�ࣨ��Ҫ�ɷ�ΪPbO��Pb��PbSO4�ȣ�Ϊԭ���Ʊ����εĹ���������ͼ��ʾ��
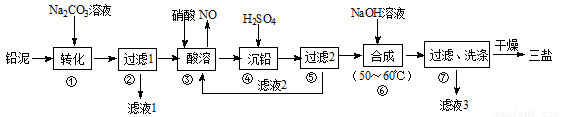
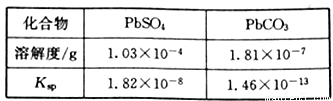
��֪��PbSO4��PbCO3���ܽ�Ⱥ��ܶȻ�Ksp���±���
��1�������ת����Ŀ����_______����Һ1�е�����ΪNa2CO3��_______���ѧʽ����
��2�����������ʱ��Ϊ����������ʣ��ɲ�ȡ�Ĵ�ʩ��_________����дһ����������Ǧ�����ᷴӦ����Pb(NO3)2��NO�����ӷ���ʽΪ__________________��
��3����Һ2�п�ѭ�����õ����ʵĻ�ѧʽΪ_______��������ܳ�Ǧ�����Һ��c(Pb2+)=1.82��10-5mol/L�����ʱc(SO42-)=______mol/L��
��4�������ϴ�Ӳ���ʱ����������Ƿ�ϴ����ȫ�ķ�����________________��
��5������ϳ����εĻ�ѧ����ʽΪ____________�����õ��������������99.Ot������Ǧ���е�ǦԪ����80��ת��Ϊ���Σ���Ǧ����ǦԪ�ص���������Ϊ________��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2017���㽭ʡ����3�¸߿�ģ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��д��ȷ���� �� ��
A. ̼��ƺ����ᷴӦ��CO32- +2H+= CO2�� +H2O
B. ��NaOH��Һ�еμ�����Ca(HCO3)2��Һ��Ca2+ +HCO3- +OH- = CaCO3��+H2O
C. ͭ�����Ȼ�����Һ��Ӧ��Cu + Fe3+ = Fe2+ + Cu2+
D. ��Ba(OH)2��Һ��H2SO4��Ӧ��Ba2+ + 2OH- + 2H+ +SO42- = BaSO4�� + 2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017��ӱ�ʡ������ѧ��������2����ѧ�Ծ��������棩 ���ͣ�ѡ����
��
��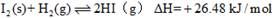
�����ж���ȷ����
A. 254g I2��g����ͨ��2g H2��g������Ӧ����9.48 kJ
B. 1 mol��̬����1 mol��̬���������������17��00 kJ
C. ��Ӧ�ٵIJ���ȷ�Ӧ�ڵIJ����ȶ�
D. ��Ӧ�ڵķ�Ӧ���������ȷ�Ӧ�ٵķ�Ӧ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017��ɽ��ʡ̩���и�����һ�ָ�ϰ������⣨һģ�������ۺϻ�ѧ�Ծ��������棩 ���ͣ������
��ΪVA��Ԫ�أ�����ұ�����̲����ĺ����ж��������账�����⡣
I��ұ����ˮ����Ԫ����Ҫ��������(H3AsO3)��ʽ���ڣ����û�ѧ�������������Ը�Ũ�Ⱥ����ˮ���乤���������£�
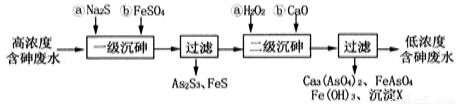
��֪����As2S3�������S2-�������·�Ӧ��As2S3(s)+3S2-(aq)  2AsS33-(aq)��
2AsS33-(aq)��
���������ε��ܽ��Դ�����Ӧ�����Ρ�
(1)����������Ԫ�صĻ��ϼ�Ϊ________������ĵ�һ�����뷽��ʽΪ_____________��
(2)��һ�����顱��FeSO4��������___________�����������顱��H2O2�뺬�����ʷ�Ӧ�Ļ�ѧ����ʽΪ_____________��
(3)����XΪ___________(�ѧʽ)��
��ұ�������е���Ԫ����Ҫ��As2S3����ʽ���ڣ����ù������鷨�붨�����(As�� ��ͼ����Ϊ3.0��10-6g)��
����1��ȡ10g������Ʒ���������п�ۻ�ϣ�����H2SO4���ȣ�����AsH3���塣
����2����AsH3����ͨ��AgNO3��Һ�У�����������As2O3��
����3��ȡ1g������Ʒ���ظ�����ʵ�飬δ���������ɡ�
(4)AsH3�ĵ���ʽΪ_______________��
(5)����2�����ӷ���ʽΪ_________________��
(6)�����������ŷű��У���Ԫ�ز��ø���4.0��10-5g��kg-1����ͨ������˵�����ŷŵķ�������Ԫ�صĺ���_______(����ϡ����������ϡ�)�ŷű���ԭ����__________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017��ɽ��ʡ̩���и�����һ�ָ�ϰ������⣨һģ�������ۺϻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ç������ijЩ�ߵ�ֲ�����е�֬��״�л��᳣������һ����ṹ��ʽ��ͼ��ʾ������˵����ȷ����
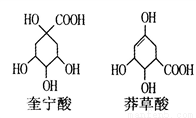
A. ��������ç���ụΪͬ���칹��
B. �����Ậ�еĹ�������ȫ��ͬ
C. ��������ܷ����ӳɷ�Ӧ���ۺϷ�Ӧ��ȡ����Ӧ
D. �����ʵ����Ŀ������ç����ֱ�������Na��Ӧ��ͬ��ͬѹ�²���H2�������Ϊ5��4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ�����и����ڶ��δ��������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����Ũ�Ȳ�������綯�Ƶĵ�س�ΪŨ���ء�������ͼ��ʾװ�ý���ʵ�飬��ʼ�ȱպ�K2���Ͽ�Kl��һ��ʱ����ٶϿ�K2���պ�Kl���γ�Ũ���أ�������ָ��ƫת��Ag+Ũ��Խ��������Խǿ��������˵������ȷ����
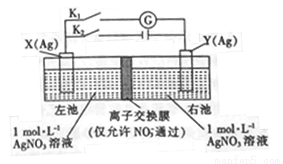
A. �պ�K2���Ͽ�Klһ��ʱ���X�缫��������
B. �պ�K2���Ͽ�Klһ��ʱ����ҳ�c(AgNO3)����
C. �Ͽ�K2���պ�K1, X �缫����������Ӧ
D. �Ͽ�K2���պ�K1, NO3-��������ҳ��ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�켪��ʡ�����и�����ѧ�ڵڶ�������������ۻ�ѧ�Ծ��������棩 ���ͣ������
2016��9�£����Ǹ���1�š��й���̨��Ĭ�ƶ�����վMFC30��ʽ������MFC30�ǻ��ڼ״���������ȼ�ϵ�ط��缼����
��1���״����ⷽʽ��Ҫ���������֣���Ӧ��״�ˮ�����������⣺CH3OH(g)+H2O(g)  CO2(g)+3H2(g) ��H1=+49.4 kJ/mol��Ӧ��״��ֽ����⣺CH3OH(g)
CO2(g)+3H2(g) ��H1=+49.4 kJ/mol��Ӧ��״��ֽ����⣺CH3OH(g) CO(g)+2H2(g) ��H2=+90.6 kJ/mol��Ӧ����̬�״�������������ͬʱ���ɶ�����̼��������
CO(g)+2H2(g) ��H2=+90.6 kJ/mol��Ӧ����̬�״�������������ͬʱ���ɶ�����̼��������
����֪CO��ȼ����Ϊ283.0 kJ/mol����Ӧ����Ȼ�ѧ��Ӧ����ʽΪ____________��
�ڸ��������ⷽʽ�У������ļ״��������������Ƿ�Ӧ____________��(�����������
��2��ʵ����ģ�ⷴӦ��״�ˮ��������������۲죬�ϳ������n(CH3OH): n(H2O)=1��1ʱ����ϵ�м״���ƽ��ת�������¶Ⱥ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��

�ٸ÷�Ӧ��ƽ�ⳣ������ʽΪ____________________��
�ڵ��¶�Ϊ250�桢ѹǿΪP2ʱ����Ӧ��ƽ��ʱH2���������Ϊ____________��
��ͼ�е�ѹǿ��С�����˳����____________��
��3��MFC30ȼ�ϵ��������Ϊȼ�ϣ�Li2CO3��K2CO3��ϵ�̼����Ϊ����ʵĸ�����ȼ�ϵ�أ��为���ĵ缫��ӦʽΪ____________��������ͨ�������Ϊ____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�����ʡ���������е�ʮ��У�ص���ѧ������һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
�о����֣�����Խϡ����ԭ�����е�Ԫ�صĻ��ϼ�Խ�͡�ijͬѧȡ�����������Ͻ���������ϡ�������ַ�Ӧ��û������ų����ڷ�Ӧ���������Һ�У���μ���4 mol/LNaOH ��Һ������NaOH��Һ�������mL��������ij��������ʵ���(mol)�Ĺ�ϵ��ͼ��ʾ������˵������ȷ����
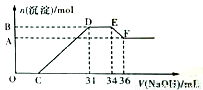
A. O����Һ�е�������Ϊ��H+��Fe2+��Fe3+��Al3+
B. DE�η�Ӧ�����ӷ���ʽΪ��NH4++OH-=NH3��H2O
C. �Ͻ��У�n(Al)=0.008mol
D. ���ⶨF�������������ʵ�鲽���ǣ����ˡ�ϴ�ӡ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�꽭��ʡ�߶�3��ѧҵˮƽ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
������Ա���ַ�����ͬλ����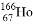 ����Ч�����Ƹΰ�����ͬλ��ԭ�Ӻ����������������֮��Ϊ�� ��
����Ч�����Ƹΰ�����ͬλ��ԭ�Ӻ����������������֮��Ϊ�� ��
A. 32 B. 67 C. 99 D. 166
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com