
| A. | 电解产物在应用中都只能作为氧化剂 | |
| B. | 电解一段时间后,溶液pH不变 | |
| C. | 阳极反应:3H2O-6e-═O3+6H+ | |
| D. | 每生成1 mol O3转移电子数为3 mol |
分析 由阳极制得臭氧,阴极制得过氧化氢.电解总方程式为:3H2O+3O2═3H2O2+O3,阳极反应为3H2O→O3+6H++6e-,阴极反应为6H++3O2+6e-→3H2O2,以此来解答.
解答 解:A、电解产物中,H2O2既可做氧化剂又可做还原剂,故A错误;
B.由电解反应可知,消耗水,则氢离子的浓度增大,pH变小,故B错误;
C.阳极上发生失电子的还原反应,即3H2O=O3+6H++6e-,故C正确;
D.由阳极反应为3H2O→O3+6H++6e-,则每生成1molO3转移电子数为6mol,故D错误;
故选C.
点评 本题为信息习题,考查电解原理,明确电解反应及阳极制得臭氧,阴极制得过氧化氢是解答本题的关键,难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | CH3-CH2-NO2和H2N-CH2-COOH互为同分异构体 | |
| B. | H、D、T互为同位素 | |
| C. | O2和O3互为同素异形体 | |
| D. | CH3CH2CH2CH3与 性质完全相同 性质完全相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
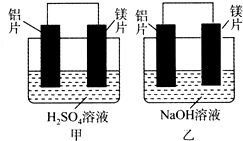 有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6 mol•L-1的H2SO4溶液中,乙同学将电极放入6 mol•L-1的NaOH溶液中,如图所示.
有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均用镁片和铝片作电极,但甲同学将电极放入6 mol•L-1的H2SO4溶液中,乙同学将电极放入6 mol•L-1的NaOH溶液中,如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 混合气体通过盛有酸性高锰酸钾溶液的洗气瓶 | |
| B. | 混合气体通过盛有足量溴水的洗气瓶 | |
| C. | 混合气体通过盛有蒸馏水的洗气瓶 | |
| D. | 混合气体通过盛有NaOH溶液的洗气瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分别加入碘水,观察颜色反应 | |
| B. | 分别加稀硫酸煮沸,再加足量NaOH溶液调至碱性,加银氨溶液加热观察有无银镜 | |
| C. | 分别加热水溶解,观察溶解性 | |
| D. | 放在嘴里咀嚼,有无甜味产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高级脂肪酸甘油酯是高分子化合物 | |
| B. | 天然的不饱和高级脂肪酸甘油酯都是混甘油酯 | |
| C. | 植物油可以使酸性高锰酸钾溶液褪色 | |
| D. | 油脂皂化完全后原有的液体分层现象消失 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
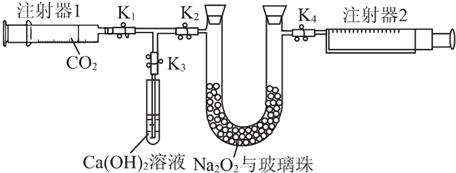
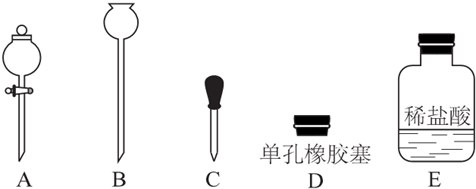
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com