
 ������ԭΪ������
������ԭΪ������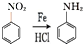
 ��
��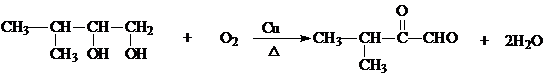 ��
�� ��
��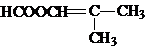 ��
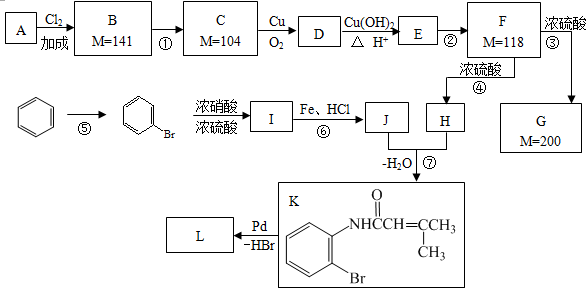
������ ����K�ĽṹΪ��λ�����屽����������Ӧ����IΪ ��I�������Ȼ��������·�����ԭ��Ӧ����JΪ
��I�������Ȼ��������·�����ԭ��Ӧ����JΪ ��J��H������ˮ����K�������K�Ľṹ����֪HΪ
��J��H������ˮ����K�������K�Ľṹ����֪HΪ ����ΪF��Ũ���������¿��Է������ֲ�ͬ�ķ�Ӧ�ֱ��γ�H��G������H����Է�������Ϊ100��FΪ118��GΪ200����F��Ũ���������·�����ȥ��Ӧ����H��2����F��Ũ������������ȥ2����ˮ�������Ӽ�������Ӧ����G����FΪ
����ΪF��Ũ���������¿��Է������ֲ�ͬ�ķ�Ӧ�ֱ��γ�H��G������H����Է�������Ϊ100��FΪ118��GΪ200����F��Ũ���������·�����ȥ��Ӧ����H��2����F��Ũ������������ȥ2����ˮ�������Ӽ�������Ӧ����G����FΪ ��GΪ
��GΪ ����A�����������ӳɷ�Ӧ����B������B����Է�������141������A����Է�������70������ʽΪC5H10��B����2����ԭ�ӣ���B��141��������Ӧ������C��104��������Է��������ó�B������������Һ�з���ˮ�ⷴӦ����C����C�к���2���ǻ�����C����������D��D�����Ƶ�������ͭ��Ӧ����E��E�ַ�Ӧ����F������F�Ľṹ��ʽ����CΪ
����A�����������ӳɷ�Ӧ����B������B����Է�������141������A����Է�������70������ʽΪC5H10��B����2����ԭ�ӣ���B��141��������Ӧ������C��104��������Է��������ó�B������������Һ�з���ˮ�ⷴӦ����C����C�к���2���ǻ�����C����������D��D�����Ƶ�������ͭ��Ӧ����E��E�ַ�Ӧ����F������F�Ľṹ��ʽ����CΪ ��DΪ
��DΪ ��EΪ
��EΪ ��BΪ
��BΪ ��AΪ
��AΪ ���ݴ˷������
���ݴ˷������
��� �⣺����K�ĽṹΪ��λ�����屽����������Ӧ����IΪ ��I�������Ȼ��������·�����ԭ��Ӧ����JΪ
��I�������Ȼ��������·�����ԭ��Ӧ����JΪ ��J��H������ˮ����K�������K�Ľṹ����֪HΪ
��J��H������ˮ����K�������K�Ľṹ����֪HΪ ����ΪF��Ũ���������¿��Է������ֲ�ͬ�ķ�Ӧ�ֱ��γ�H��G������H����Է�������Ϊ100��FΪ118��GΪ200����F��Ũ���������·�����ȥ��Ӧ����H��2����F��Ũ������������ȥ2����ˮ�������Ӽ�������Ӧ����G����FΪ
����ΪF��Ũ���������¿��Է������ֲ�ͬ�ķ�Ӧ�ֱ��γ�H��G������H����Է�������Ϊ100��FΪ118��GΪ200����F��Ũ���������·�����ȥ��Ӧ����H��2����F��Ũ������������ȥ2����ˮ�������Ӽ�������Ӧ����G����FΪ ��GΪ
��GΪ ����A�����������ӳɷ�Ӧ����B������B����Է�������141������A����Է�������70������ʽΪC5H10��B����2����ԭ�ӣ���B��141��������Ӧ������C��104��������Է��������ó�B������������Һ�з���ˮ�ⷴӦ����C����C�к���2���ǻ�����C����������D��D�����Ƶ�������ͭ��Ӧ����E��E�ַ�Ӧ����F������F�Ľṹ��ʽ����CΪ
����A�����������ӳɷ�Ӧ����B������B����Է�������141������A����Է�������70������ʽΪC5H10��B����2����ԭ�ӣ���B��141��������Ӧ������C��104��������Է��������ó�B������������Һ�з���ˮ�ⷴӦ����C����C�к���2���ǻ�����C����������D��D�����Ƶ�������ͭ��Ӧ����E��E�ַ�Ӧ����F������F�Ľṹ��ʽ����CΪ ��DΪ
��DΪ ��EΪ
��EΪ ��BΪ
��BΪ ��AΪ
��AΪ ��
��
��1���������Ϸ�������Ӧ��ΪF��Ũ���������·�����ȥ��Ӧ����H����Ӧ��ΪI�������Ȼ��������·�����ԭ��Ӧ����J���ʴ�Ϊ����ȥ��Ӧ����ԭ��Ӧ��
��2���������Ϸ�������Ӧ��ΪB������������Һ���������·���ˮ�ⷴӦ����C����Ӧ��Ϊ����Һ�壬���������������·���ȡ����Ӧ�����屽���ʴ�Ϊ��NaOHˮ��Һ�����ȣ�Һ�壬���ۣ�
��3��JΪ �������������ǰ�������ԭ�ӣ��ʴ�Ϊ����������ԭ�ӣ�
�������������ǰ�������ԭ�ӣ��ʴ�Ϊ����������ԭ�ӣ�
��4���������Ϸ�����AΪ ������Ϊ3-��-1-��ϩ����������K������Ϣ��Ӧ����L����LΪ
������Ϊ3-��-1-��ϩ����������K������Ϣ��Ӧ����L����LΪ ���ʴ�Ϊ��3-��-1-��ϩ��
���ʴ�Ϊ��3-��-1-��ϩ�� ��
��
��5��C������������Ӧ����D��C��D��
D�����Ƶ�Cu��OH��2����������Ӧ����Ӧ����ʽΪ��CH3��2CHCOCHO+2Ag��NH3��2OH$\stackrel{��}{��}$��CH3��2CHCOCOONH4+2Ag��+3NH3+H2O��
F��G�� ��
��
�ʴ�Ϊ��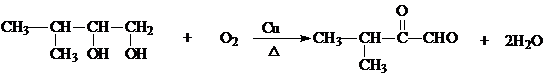
 ��
��
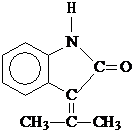
��6��HΪ ���ж���ͬ���칹��i���ܷ���ˮ�ⷴӦ��˵������������ii��������ֻ����������iii��������״�ṹ�����Է��������Ľṹ��ʽΪ��
���ж���ͬ���칹��i���ܷ���ˮ�ⷴӦ��˵������������ii��������ֻ����������iii��������״�ṹ�����Է��������Ľṹ��ʽΪ��

���� ���⿼���л����ƶϣ�Ϊ��Ƶ���㣬���ؿ���ѧ�������ƶ����������ݷ�Ӧ��������Ӧǰ�����ʽṹ��ʽ�仯��������Ϣ�����ƶϣ���ȷ�ƶ��л���ṹ��ʽ�ǽⱾ��ؼ�����Ŀ�Ѷ��еȣ�


 �Ƹ�С״Ԫ�������������ϵ�д�
�Ƹ�С״Ԫ�������������ϵ�д� ����һ������ܼƻ�ϵ�д�
����һ������ܼƻ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | OH- | B�� | Ba2+ | C�� | NO3- | D�� | CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | C��O2����ʱ�������ķ�Ӧ��Ҫ�Ƿ��ȷ�Ӧ | |
| B�� | úȼ��ʱ���������Խ��Խ�� | |
| C�� | CO2+C$\frac{\underline{\;����\;}}{\;}$2CO��һ��Ӧ�������ȷ�Ӧ | |
| D�� | úȼ��ʱ����Ӧ���������������������������������Էų����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
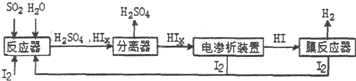
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
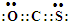 ��
��
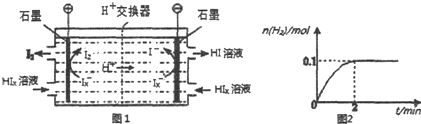
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 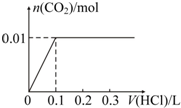 | B�� | 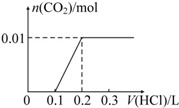 | ||
| C�� | 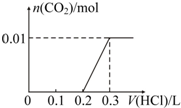 | D�� | 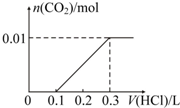 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���ˮ�м��������ƾ������Խ��ⵥ����ȡ���� | |
| B�� | ����ʱ��Ӧʹ�¶ȼ�ˮ����������ƿ֧�ܿ� | |
| C�� | ��Һʱ����Һ©���²�Һ����¿ڷų����ϲ�Һ����Ͽڵ��� | |
| D�� | ����ʱ������Һ�г��ִ�������ʱ��ֹͣ������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
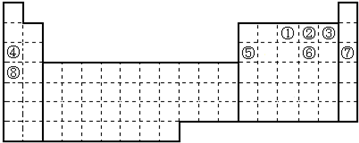
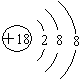 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com