
(14分) (1)322g Na2SO4·10H2O的物质的量是________,其中所含的Na+的物质的量是 ,所含H2O分子的数目是 个;将322gNa2SO4·10H2O溶于水配成2L溶液,其物质的量浓度是_______ 。
(2)现有m g某气体,它由双原子分子构成,它的摩尔质量为M g·mol-1。若阿伏加德罗常数用NA表示,则:
①该气体的物质的量为 mol。
②该气体在标准状况下的体积为 L。
③该气体溶于水后形成V L溶液,其溶液的物质的量浓度为 mol/L
科目:高中化学 来源: 题型:
实验室欲配制100 mL0.92 mol•L-1的H2SO4溶液(本小题每空2分,共14分)
(1)需要用到的仪器,除了烧杯、空试剂瓶、玻璃棒、量筒、还必须有 ;
(2)若提供的是18.4 mol•L-1的浓H2SO4,求所需量取的浓H2SO4的体积为 mL;
(3)对配制过程中的下列说法,正确的是 。(填序号,多选、少选均不得分)
A.量筒量取浓硫酸后要冲洗并将冲洗液一起倒入小烧杯
B.量好体积的浓硫酸应先倒入小烧杯中然后再加水稀释
C.稀释好的稀硫酸要立即转移入容量瓶
D.若定容后摇匀液面又下降了。则必须再补加水至刻度线。
(4)配制稀硫酸的容量瓶必须洗涤,若用含有蒸馏水的容量瓶未干燥就配制稀硫酸,
则所配稀硫酸浓度将 (偏高、偏低、不变);若用刚配制过NaOH
溶液的容量瓶未洗涤就配制稀硫酸,则所配制的稀硫酸溶液的浓度将
(偏高、偏低、不变);若用刚配制过HCl溶液的容量瓶未洗涤就配制稀硫酸,则
所配制稀硫酸浓度将 (偏高、偏低、不变),
氢离子浓度将 (偏高、偏低、不变)。
查看答案和解析>>
科目:高中化学 来源:2013届山东省济宁市泗水一中高三上学期期末模拟化学试卷(带解析) 题型:填空题
(14分)
Ⅰ.(1)分析下表中各项的排布规律,按此规律排布第22项应为 。
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| C2H4 | C2H6 | C2H6O | C2H4O2 | C3H6 | C3H8 | C3H8O | C3H6O2 | C4H8 | C4H10 |
查看答案和解析>>
科目:高中化学 来源:2014届安徽省高二第二次月考化学试卷(解析版) 题型:填空题
(14分)取0.1 mol/L HA溶液与0.1 mol/L NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8。试回答以下问题:
(1)混合溶液的pH=8的原因是________________________________(用离子方程式表示)。
(2)混合溶液中由水电离出的c(H+)________0.1 mol/L NaOH溶液中由水电离出的c(H+) (填“>”、“<”或“=”)。
(3)求出混合液中下列算式的精确计算结果(填具体数字):
c(Na+)-c(A-)=________mol/L;c(OH-)-c(HA)=________mol/L。
(4)已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH________7(填“>”、“<”或“=”)。
(5)有相同温度下相同浓度的四种盐溶液:A.NH4HCO3;B.NH4A;C.(NH4)2SO4;D.NH4Cl,按pH由大到小的顺序排列________(填序号)。
查看答案和解析>>
科目:高中化学 来源:2010年湖北省高二12月月考化学试卷 题型:选择题
某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,生成4mol z时放出热量Q KJ, 它们的物质的量随时间的变化如表所示。
|
t/min |
X/mol |
Y/mol |
Z/mol |
|
0 |
1.00 |
1.00 |
0.00 |
|
1 |
0.90 |
0.80 |
0.20 |
|
3 |
0.75 |
0.50 |
0.50 |
|
5 |
0.65 |
0.30 |
0.70 |
|
9 |
0.55 |
0.10 |
0.90 |
|
10 |
0.55 |
0.10 |
0.90 |
|
14 |
0.55 |
0.10 |
0.90 |
(1)根据上表中数据,在答卷该题相应位置上画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:
(2) 写出体系中发生反应的热化学方程式 ______;
(3) 列式计算该反应在0-3min时间内产物Z的平均反应速率:
(4) 该反应达到平衡时反应物X的转化率 等于______________________;
等于______________________;
(5) 改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线1、2、3(如下图所示)则曲线1、2、3所对应的实验条件改变分别是:1 _____2_____3_____的曲线:

查看答案和解析>>
科目:高中化学 来源:2010年广东省高二上学期期中考试化学卷 题型:填空题
某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,生成4mol z时放出热量Q KJ, 它们的物质的量随时间的变化如表所示。
|
t/min |
X/mol |
Y/mol |
Z/mol |
|
0 |
1.00 |
1.00 |
0.00 |
|
1 |
0.90 |
0.80 |
0.20 |
|
3 |
0.75 |
0.50 |
0.50 |
|
5 |
0.65 |
0.30 |
0.70 |
|
9 |
0.55 |
0.10 |
0.90 |
|
10 |
0.55 |
0.10 |
0.90 |
|
14 |
0.55 |
0.10 |
0.90 |
(1)根据上表中数据,在答卷该题相应位置上画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:
(2) 写出体系中发生反应的热化学方程式 ______;
(3) 列式计算该反应在0-3min时间内产物Z的平均反应速率:
(4) 该反应达到平衡时反应物X的转化率 等于______________________;
等于______________________;
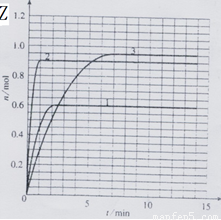
(5) 改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线1、2、3(如下图所示)则曲线1、2、3所对应的实验条件改变分别是:1 _____2_____3_____的曲线:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com