
【题目】某化学兴趣小组利用如图装置制取氨气并探究氨气的有关性质。

(1)装置A中烧瓶内试剂可选用_______(填序号)。
a.碱石灰 b.浓硫酸 c.生石灰 d.五氧化二磷 e.烧碱固体
(2)若探究氨气的溶解性,需在K2的导管末端连接下表装置中的_____(填序号)装置,当装置D中集满氨气后,关闭K1、K2,打开K3,引发喷泉的实验操作是________。
备选装置(其中水中含酚酞溶液) | ||
|
|
|
Ⅰ | Ⅱ | Ⅲ |
(3)若探究氨气的还原性,需打开K1、K3,K,2处导管连接制取纯净、干燥氯气的装置。
①用二氧化锰与浓盐酸制取氯气生成气体必须通过盛有_____试剂的洗气瓶;
②D中氨气与氯气反应产生白烟,同时生成一种无色无味的气体,该反应的化学方程式为_________。
③从K3处导管逸出的气体中含有少量C12,则C装置中应盛放_____溶液(填化学式),反应的离子方程式为___________。
【答案】 ace II或III 用热毛巾将烧瓶捂热片刻(其他合理答案均可) 饱和食盐水、浓硫酸 3C12+8NH3=6NH4Cl+N2 NaOH Cl2+2OH-=Cl-+ClO-+H2O
【解析】(1)氨水易挥发,升高温度能促进氨水分解生成氨气,为促进氨水分解,则烧瓶中加入的物质遇氨水后能放出大量热,且和氨水不反应,装置A中烧瓶内试剂可选用:a.碱石灰遇水放出大量热,能使氨水温度升高,且和氨水不反应,故a选; b.浓硫酸和氨水反应,故b不选; c.生石灰遇水放出大量热,能使氨水温度升高,且和氨水不反应,故c选;d.五氧化二磷与水反应生成磷酸,和氨水反应,故d不选;e.烧碱固体遇水放出大量热,能使氨水温度升高,且和氨水不反应,故e选;故选 ace ;(2)利用压强差将烧杯中的水排到烧瓶中,操作为用热毛巾将烧瓶捂热,烧瓶中的空气进入烧杯中,导致大气压强大于烧瓶中气体压强,从而使烧杯中的水通过导管进入烧瓶中产生喷泉实验,氨气极易溶于水,为防止倒吸,吸收氨气的装置中应该有缓冲装置,Ⅱ、Ⅲ装置中都有缓冲装置,Ⅰ没有缓冲装置能产生倒吸,不能在K2的导管末端连接图乙中的 I;要引发喷泉,用热毛巾将烧瓶捂热片刻(其他合理答案均可)。(3)①浓盐酸制取的氯气中含有氯化氢气体和水蒸气,为防止干扰实验,氯气在进入烧瓶前,应该用饱和食盐水和浓硫酸除去氯化氢和水蒸气;②根据氧化还原反应知,生成的无色无味的气体是氮气,所以其反应方程式为:3Cl2+8NH3=6NH4Cl+N2,③氯气和水反应生成盐酸和次氯酸导致氯气的水溶液呈酸性,所以可以用氢氧化钠溶液除去氯气,反应离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O。


科目:高中化学 来源: 题型:
【题目】下列鉴别方法不可行的是( )
A.用水鉴别乙醇、甲苯和溴苯
B.用燃烧法鉴别乙醇、苯和四氯化碳
C.用澄清石灰水溶液鉴别苏打、小苏打
D.用酸性高锰酸钾溶液鉴别苯、环己烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C和D是同一周期的四种元素,A、B、C的原子序数依次相差1;A元素的单质化学性质最活泼,能与水直接发生反应.B元素的氧化物2.0g恰好跟100mL0.5mol/L的H2SO4完全反应.B元素的单质跟D元素单质反应生成BD2型化合物.根据以上事实回答:
(1)A原子的结构示意图为
(2)C在周期表中的位置:
(3)BD2含有的化学键类型为
(4)A,C两元素最高价氧化物的水化物相互反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应:SO2(g)+NO2(g)![]() SO3(g)+NO(g) ,达到平衡,正反应速率随时间变化如图所示。则正确的结论是
SO3(g)+NO(g) ,达到平衡,正反应速率随时间变化如图所示。则正确的结论是
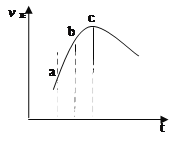
A. 逆反应速率:a点小于点c
B. 反应物浓度:a点小于点b
C. 反应在c点时处于平衡状态
D. 反应物的总能量低于生成物的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化硅有晶体和无定形两种形态,晶态二氧化硅主要存在于石英矿中.除石英外,SiO2还有磷石英和方英石等多种变体.方英石结构和金刚石相似,其结构单元如图.下列有关说法正确的是( ) 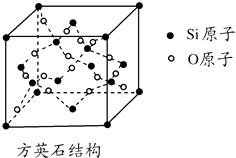
A.方英石晶体中存在着SiO4结构单元
B.1 mol Si形成2 mol Si﹣O键
C.上图所示的结构单元中实际占有18个硅原子
D.方英石晶体中,Si﹣O键之间的夹角为90°
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在含有Ag+的酸性溶液中,以铁铵矾NH4Fe(SO4)2作指示剂,用KSCN的标准溶液滴定Ag+.已知:AgSCN(白色s)![]() Ag++SCN-,Ksp=1.0×10-12;Fe3++SCN-
Ag++SCN-,Ksp=1.0×10-12;Fe3++SCN-![]() [Fe(SCN)] 2+(红色),K=138。下列说法不正确的是( )
[Fe(SCN)] 2+(红色),K=138。下列说法不正确的是( )
A. 边滴定,边摇动溶液,溶液中首先析出AgSCN白色沉淀
B. 当Ag+定量沉淀后,少许过量的SCN-与Fe3+生成红色配合物,即为终点
C. 上述实验可用KCl标准溶液代替KSCN的标准溶液滴定Ag+
D. 滴定时,必须控制溶液一定的酸性,防止Fe3+水解,影响终点的观察
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大,以下是某温度下这四种酸在冰醋酸中的电离常数
酸 | HClO4 | H2SO4 | HCl | HNO3 |
Ka] | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
从以上表格中判断以下说法中不正确的是( )
A.在冰醋酸中硫酸的电离方程式为H2SO4=2H++SO![]()
B.在冰醋酸中高氯酸是这四种酸中最强的酸
C.在冰醋酸中这四种酸都没有完全电离
D.水对于这四种酸的强弱没有区分能力,但醋酸可以区别这四种酸的强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图分别表示生物体内的生物大分子的部分结构模式图,据图回答下列问题:
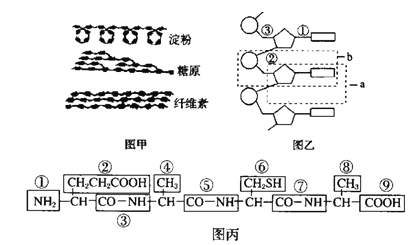
(1)图甲中的三种物质的基本单位都是___________,其中属于动物细胞储能物质的是___________。这三种物质中,在功能上与另外两种截然不同的是______________________。
(2)图乙化合物是肺炎双球菌遗传物质的一部分,其基本单位是__________,可用图中字母_______表示,各基本单位之间是通过___________(填①、②或③)连接起来的。
(3)图丙所示化合物的名称是___________,是由___________种氨基酸经___________过程形成的,脱去水中的氢元素来自___________,连接氨基酸之间的化学键是___________(填化学键结构)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟化钡可用于制造电机电刷、光学玻璃、光导纤维、激光发生器。以钡矿粉(主要成分为BaCO3,含有SiO2、Fe2+、Mg2+等杂质)制备氟化钡的流程如下:
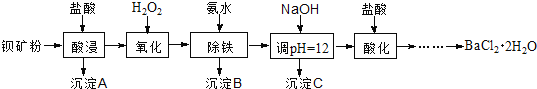
已知:常温下Fe3+、Mg2+完全沉淀的pH分别是:3.4、12.4。
(1)滤渣A的名称为___________。
(2)滤液1加H2O2的目的是___________。
(3)加NaOH溶液调节pH=12.5,得到滤渣C的主要成分是___________(写化学式)
(4)滤液3加入盐酸酸化后再经加热浓缩____________洗涤,真空干燥等一系列操作后得到BaCl2·2H2O晶体。
(5)常温下,用BaCl2·2H2O配制成0.2 mol/L水溶液与氟化铵溶液反应,可得到氟化钡沉淀。请写出该反应的离子方程式___________。已知Ksp(BaF2)=1.84×10-7,当钡离子完全沉淀时(即钡离子浓度≤10-5 mol/L),至少需要的氟离子浓度是___________mol/L(已知![]() =1.36,计算结果保留三位有效数字)。
=1.36,计算结果保留三位有效数字)。
(6)5.0 t含80%BaCO3的钡矿粉,理论上最多能生成BaCl2·2H2O晶体___________t 。(保留2位小数)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com