
【题目】MnO2是碱锰电池材料中最普通的正极材料之一,在活性材料MnO2中加入CoTiO3纳米粉体,可以提高其利用率,优化碱锰电池的性能。
(1)写出基态Mn原子的价电子排布式_____________,基态Mn原子核外电子的运动状态有___种;
(2)①CoTiO3晶体结构模型如图1所示,晶胞参数a=0.53nm。在CoTiO3晶体中1个Ti原子、1个Co原子周围距离最近的O原子数目分别为________个、________个。
②列式表示CoTiO3晶体的密度:________g.cm-3(不必计算出结果,用NA表示阿伏加德罗常数的值)。
(3)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂,常用于污水处理。O2在其催化作用下,可将CN-氧化成CNO-,进而得到N2。与CNO- 互为等电子体的分子、离子化学式分别为___________、___________(各写一种)。
(4)三聚氰胺是一种含氮化合物,其结构简式如图2所示。
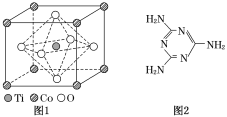
三聚氰胺分子中氮原子轨道杂化类型是____________,1 mol三聚氰胺分子中σ键的数目为________。
【答案】3d54s225612(1×155)/[NA× (a×10-7)3]CO2(或N2O、CS2、BeCl2等合理均可)N![]() sp2、sp315NA
sp2、sp315NA
【解析】
(1)Mn为25号元素,根据电子排布规律可得电子排布式。
(2)观察CoTiO3晶体结构模型图,可知1个Ti原子周围距离最近的O原子数目分别为6个、1个Co原子周围距离最近的O原子数目为12个。
(3)等电子体为原子数目相等、价电子数相等。
(4)-NH2中N形成了三个单键为SP3杂化,环中N原子形成了一个单键和一个双键,为SP2杂化,1个三聚氰胺分子含15个σ键,所以1 mol三聚氰胺分子中 σ键的数目为15NA
(1)Mn是25号元素,其原子核外有25个电子,根据构造原理书写其基态原子核外电子排布式为1s22s22p63s23p63d54s2;每个电子都有1种运动状态,Mn原子核外有25个电子,所以共有25种运动状态。(2)①根据CoTiO3晶体结构模型图,在CoTiO3晶体中,1个Ti原子周围距离最近的O原子个数是6,1个Co原子周围距离最近的O原子数目=3×8÷2=12个;根据均摊原则,每个晶胞中Co原子数是![]() 、Ti原子数是1、O原子数是
、Ti原子数是1、O原子数是![]() ,晶胞的摩尔质量是155g/mol,一个晶胞的体积是a×10-7)3cm3,所以晶体的密度是(1×155)/[NA× (a×10-7)3] g.cm-3;(3)原子个数相等、价电子数相等的微粒互为等电子体,所以与CNO-互为等电子体的分子、离子化学式分别为CO2(或N2O、CS2、BeCl2等)、N3-;(4)氨基上N原子价层电子对个数是4,则N原子采用sp3杂化;环中N原子形成了一个单键和一个双键, N原子采用sp2杂化; 1个三聚氰胺分子中σ键个数是15,所以1mol三聚氰胺分子中σ键的数目为15NA。
,晶胞的摩尔质量是155g/mol,一个晶胞的体积是a×10-7)3cm3,所以晶体的密度是(1×155)/[NA× (a×10-7)3] g.cm-3;(3)原子个数相等、价电子数相等的微粒互为等电子体,所以与CNO-互为等电子体的分子、离子化学式分别为CO2(或N2O、CS2、BeCl2等)、N3-;(4)氨基上N原子价层电子对个数是4,则N原子采用sp3杂化;环中N原子形成了一个单键和一个双键, N原子采用sp2杂化; 1个三聚氰胺分子中σ键个数是15,所以1mol三聚氰胺分子中σ键的数目为15NA。


 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列叙述正确的是
A. 在标准状况下,11.2L O2和22.4L NO混合并充分反应后得到的气体的分子数为NA
B. 常温下0.1mol·L-1NH4NO3溶液中的氮原子数为0.2NA
C. 1mol Na与足量O2反应,生成Na2O和Na2O2的混合物,转移的电子数为NA
D. 25℃时,1.0L pH=13的Ba(OH)2溶液中,含有的OH-数目为0.2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,Ksp[Mg(OH)2]=1.1×10-11, Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.9×10-12,下列叙述不正确的是( )
A. 浓度均为2×10-5mol/L的AgNO3溶液和NaCl溶液等体积混合,有白色沉淀生成
B. 将0.001mol/L的AgNO3溶液滴入浓度均为0.001mol/L的KCl和K2CrO4混合溶液中,先产生AgCl沉淀
C. c(Mg2+)为0.11mol/L的溶液中要产生Mg(OH)2沉淀,溶液的pH要控制在9以上
D. 其他条件不变时,向饱和Ag2CrO4水溶液中加入少量K2CrO4固体,溶液中c(Ag+)减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列所给的化学反应中,不属于氧化还原反应的是
A. CaCO3+2HCl = CaCl2+CO2↑+H2O
B. Fe+CuSO4 =Cu+FeSO4
C. Fe2O3+3CO![]() 2Fe+3CO2↑
2Fe+3CO2↑
D. 2Cl2+2Ca(OH)2 = CaCl2+Ca(ClO)2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中,属于消去反应的是 ( )
A. 乙烷与溴水的反应
B. 一氯甲烷与KOH的乙醇溶液混合加热
C. 氯苯与NaOH水溶液混合加热
D. 溴丙烷与KOH的乙醇溶液混合加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E都含X元素,其转化关系如图所示:
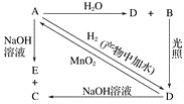
(1)请分别写出下列物质的化学式(如为溶液请填溶质的化学式):A________、B________、D________。
(2)写出下列反应的化学方程式或离子方程式(请注明反应条件):A+H2O(离子方程式):_________;A+NaOH(离子方程式):_______________;D→A(化学方程式):____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
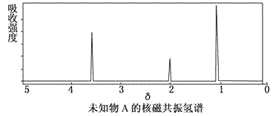
【题目】某有机物A的红外光谱和核磁共振氢谱图如下图所示,下列说法中错误的是
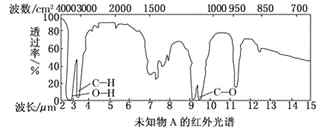
A. 由红外光谱可知,该有机物中至少有三种不同的化学键
B. 若A的化学式为C2H6O,则其结构简式为CH3—O—CH3
C. 仅由其核磁共振氢谱图无法得知其分子中的氢原子总数
D. 由核磁共振氢谱图可知,该有机物分子中有三种不同的氢原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对电负性的理解不正确的是( )
A.电负性是人为规定的一个相对数值,不是绝对标准
B.元素电负性的大小反映了元素原子对键合电子吸引力的大小
C.元素的电负性越大,则元素的非金属性越强
D.元素的电负性是元素固有的性质,与原子结构无关
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com