
| A. | 水凝结成冰 | B. | 天然气燃烧 | ||
| C. | 盐酸与氢氧化钠中和反应 | D. | 液氨气化 |
分析 物质在溶解时经常伴随有吸热或放热现象,氢氧化钠固体、浓硫酸溶于放出大量的热,温度升高;硝酸铵固体溶于水吸热,温度降低,电离、水解都是吸热过程;
常见的放热反应有:所有的物质燃烧、所有金属与酸反应、金属与水反应,所有中和反应;绝大多数化合反应和铝热反应;
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),少数分解置换以及某些复分解(如铵盐和强碱),以此解答该题.
解答 解:A.水凝结成冰,释放能量,故A不选;
B.物质燃烧属于放热过程,故B不选;
C.中和反应为放热反应,故C不选;
D.液氨气化,由液态变为气态,需要吸热,故D选.
故选D.
点评 本题考查化学中吸热或放热问题,为高频考点,侧重考查学生的双基,熟记吸热或放热的判断规律是正确解答此类题的关键,对于特殊过程中的热量变化的要熟练记忆,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 19gNHD2和19gNH2T中含有的中子数均为10NA | |
| B. | 标准状况下,22.4LO2参加反应转移的电子数一定是4NA | |
| C. | 1molCnH2n中含有的共用电子对数为(3n+1)NA | |
| D. | 2molSO2和1molO2在一定条件下充分反应后,所得混合气体的分子数大于2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
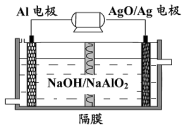 铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示.电池反应为:2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O下列说法中错误的是( )
铝电池性能优越,Al-AgO电池可用作水下动力电源,其原理如图所示.电池反应为:2Al+3AgO+2NaOH=2NaAlO2+3Ag+H2O下列说法中错误的是( )| A. | 该装置可实现化学能向电能的转化 | B. | 电池工作时AgO得到电子 | ||
| C. | Al是负极 | D. | OH-透过隔膜向AgO/Ag极迁移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用CCl4将溴从溴水中提取出来 | |
| B. | 用丁达尔效应鉴别淀粉胶体和食盐溶液 | |
| C. | 采用加热的方法除去碳酸钠固体中混有的碳酸氢钠 | |
| D. | 向某无色溶液中加入硝酸银产生白色沉淀,证明溶液中含有Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验时坩埚未完全干燥 | B. | 加热后固体颜色有少量变黑 | ||
| C. | 加热过程中晶体有少量溅失 | D. | 加热后固体未放入干燥器中冷却 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通过浓硫酸除去SO2中的H2O | B. | 通过灼热的CuO除去H2中的CO | ||
| C. | 通过灼热的镁粉除去N2中的O2 | D. | 通过碱石灰除去O2中的NH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com