
| A. | 氢化物的通式为 RH5 | B. | 最高化合价是+5 价 | ||
| C. | 非金属性由上到下递增 | D. | 其最高价含氧酸均为强酸 |
科目:高中化学 来源: 题型:解答题
 或Na+[:H]-(写一例)
或Na+[:H]-(写一例)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(A)=0.15mol/(L•min) | B. | v(B)=0.01mol/(L•s) | ||
| C. | v(C)=0.40mol/(L•min) | D. | v(D)=0.45mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{17}^{35}$Cl和${\;}_{17}^{37}$Cl | B. | ${\;}_{19}^{40}$ K 和${\;}_{20}^{40}$ Ca | ||
| C. | O2 和 O3 | D. | H2O 和 D2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 通入 H2电极是负极 | |
| B. | 通入 O2电极发生氧化反应 | |
| C. | 氢氧燃料电池是一种具有应用前景的绿色电源 | |
| D. | 氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O2和S2O32-是氧化剂,Fe2+是还原剂 | |
| B. | 每生成1 mol Fe3O4,则转移电子数为2 mol | |
| C. | 参加反应的氧化剂与还原剂的物质的量之比为1:1 | |
| D. | 若有2 mol Fe2+被氧化,则被Fe2+还原的O2为0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y元素最高价氧化物对应的水化物化学式为H3YO4 | |
| B. | 原子半径由大到小的顺序为W>Z>Y>X | |
| C. | X、Z两种元素的氧化物中所含化学键类型相同 | |
| D. | 与同浓度的盐酸反应,Z比W更剧烈 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
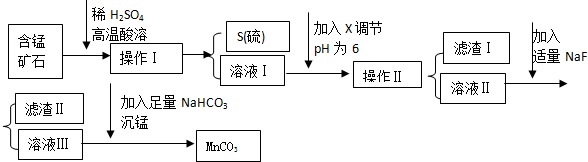
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Ca(OH)2 | 12 | ------ |
| Al(OH)3 | 3.8 | 4.7 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com