
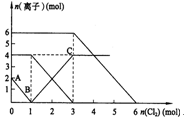
| A.还原性:I— >Fe2+>Br— |
| B.原混合溶液中FeBr2的物质的量为6mol |
| C.当通入2molCl2时,溶液中已发生的离子反应可表示为: 2Fe2++2I-+2Cl2===2Fe3++I2+4Cl- |
| D.原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3 |


 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源:不详 题型:单选题
| A.钠和铁一样,都能在氯气中燃烧生成金属氯化物 |
| B.液氯是氯气的水溶液,它能使干燥的有色布条褪色 |
| C.氯气跟变价金属反应生成高价金属氯化物 |
| D.氯水具有杀菌、漂白作用是因为氯水中含有强氧化性的次氯酸 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.等于0.3摩 | B.小于0.3摩 |
| C.大于0.3摩,小于0.6摩 | D.以上结论都不正确 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.新制氯水能使紫色石蕊试液先变红,后褪色 |
| B.氯水光照时有气泡溢出,该气体一定是氯气 |
| C.新制氯水中只有氯气和水分子 |
| D.氯水放置数天后,酸性减弱 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

| A.D装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为CO2和HCl。试写出D中反应的化学方程式:。装置C的作用是。 (3)在E处,紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是。 (4)若将E处烧杯中溶液改为澄清石灰水,反应过程现象为。(填代号) | ||
| B.有白色沉淀生成 | C.无现象 | D.先生成白色沉淀,而后白色沉淀消失 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Cl2 | B.SO2 | C.NaClO | D.KMnO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com