
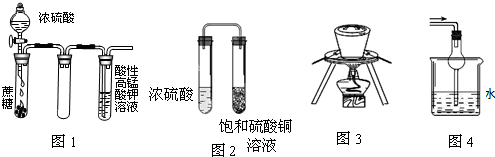
| A、图1酸性KMnO4溶液中没有气泡出现,但溶液颜色会逐渐变浅乃至褪去 |
| B、图2久置后,饱和硫酸铜溶液可能析出蓝色晶体 |
| C、图3在海带提碘实验中用于灼烧海带 |
| D、图4可用于吸收易溶于水的尾气 |


 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案科目:高中化学 来源: 题型:
| A、工业废水、废物的任意排放 |
| B、农业上大量施用农药和化肥 |
| C、用第四代广谱杀菌消毒剂的ClO2对水进行消毒杀菌 |
| D、生活中大量使用含磷洗衣粉,并把污水随意排放 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2.4g金属镁与足量盐酸反应,转移电子的数目为0.1NA |
| B、1mol/L的CaCl2溶液中含Cl-的数目为2NA |
| C、常温常压下,1.7gNH3中含N-H键数目为0.3 NA |
| D、标准状况下,11.2 L H2O含有的电子数为5 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验编号 | V(烧碱溶液)/mL | V(HCl)/mL | |
| 初读数 | 末读数 | ||
| 1 | 20.00 | 0.80 | 21.00 |
| 2 | 20.00 | 1.00 | 20.80 |
| 3 | 20.00 | 0.20 | 22.80 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、生成SO3 2 mol |
| B、放出 197 kJ 的热量 |
| C、SO2 的转化率为100% |
| D、平衡时压强不再改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 滴定次数 实验数据 | 1 | 2 | 3 | 4 |
| V(样品)/mL | 20.00 | 20.00 | 20.00 | 20.00 |
| V (盐酸)/mL(初始) | 0.00 | 0.20 | 0.10 | 0.10 |
| V (盐酸)/mL(终点) | 20.98 | 21.22 | 21.10 | 21.12 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含有AlO2-的溶液中:Na+、Al3+、NO3-、Cl- |
| B、使淀粉碘化钾变蓝的溶液中:K+、HCO3-、S2-、SO42- |
| C、能与金属铝反应放出氢气的溶液中:K+、NO3-、Cl-、Na+ |
| D、通有SO2的溶液中:Fe2+、Mg2+、Cl-、SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com