
| A. | 碘化氢的生成速率大于其分解速率 | B. | 碘化氢的生成速率等于其分解速率 | ||
| C. | 加催化剂不会影响达到平衡的时间 | D. | 升高温度可以加快平衡状态的到达 |
分析 在平衡建立过程中,反应向正反应方向移动,正反应速率大于逆反应速率;催化剂能同等程度的增大正逆反应速率,升高温度加快反应速率,据此分析解答.
解答 解:A.在平衡建立过程中,反应向正反应方向移动,正反应速率大于逆反应速率,所以HI的分解速率大于生成速率,故A错误;
B.根据A知,正逆反应速率大于逆反应速率,故B错误;
C.催化剂能同等程度的改变正逆反应速率,所以改变反应到达平衡的时间,故C错误;
D.升高温度,正逆反应速率都增大,缩短反应到达平衡的时间,所以可以加快平衡状态的到达,故D正确;
故选D.
点评 本题考查化学反应速率的影响因素,明确改变条件对反应速率的影响关系是解本题关键,注意催化剂只影响反应速率不影响平衡移动,为易错点.


 作业辅导系列答案
作业辅导系列答案科目:高中化学 来源: 题型:解答题
| 元素编号 | 元素性质或原子结构 |
| A | 有三个电子层,K、M层电子数之和等于L层电子数 |
| B | 短周期中金属性最强 |
| C | 常温下单质为双原子分子,氢化物的水溶液呈碱性 |
| D | 元素最高正价是+7价 |
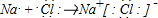 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
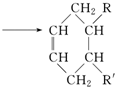 (可表示为
(可表示为 )其中,R、R′表示原子或原子团.
)其中,R、R′表示原子或原子团.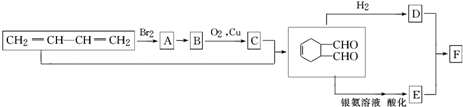
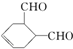 中官能团的名称是醛基.1mol该物质完全燃烧需消耗O26.5mol
中官能团的名称是醛基.1mol该物质完全燃烧需消耗O26.5mol .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 相对原子质量和核外电子数 | B. | 电子层数和最外层电子数 | ||
| C. | 相对原子质量和最外层电子数 | D. | 电子层数和次外层电子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O | B. | H2→2H | ||
| C. | CaO+H2O=Ca(OH)2 | D. | 2Cl→Cl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com