
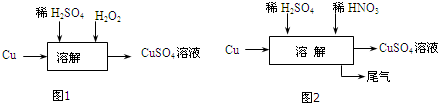
分析 方案一:第一个方案中放出的有毒气体二氧化硫会造成对空气的污染;第二个方案铜和氧气加热生成氧化铜,氧化铜和硫酸反应产生硫酸铜和水,因此反应过程中没有污染物,且原料的利用率高,方案二的实验中,发现容器底部残留少量紫红色固体,为铜,不溶于稀硫酸;
方案二:(1)方案三的实验流程如图1中,双氧水反应氧化还原反应生成O2;随着反应的进行,生成气体速度加快,可能是反应产生的Cu2+对H2O2分解有催化作用;
(2)取H2O2溶液,向其中滴加CuSO4溶液,如果产生气泡的速率加快,则证明Cu2+对H2O2分解有催化作用,否则,没有;
(3)根据离子方程式,3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,反应消耗2mol硝酸,生成3mol硫酸铜,故为了得到较纯净的硫酸铜溶液,硫酸和硝酸的物质的量之比应为3:2;
(4)设计实验方案时,为防止NO污染空气,应通入空气氧化NO为NO2,用水吸收后,生成HNO3再循环利用.
解答 解:方案一:第一个方案中放出的有毒气体二氧化硫会造成对空气的污染;第二个方案铜和氧气加热生成氧化铜,氧化铜和硫酸反应产生硫酸铜和水,因此反应过程中没有污染物,且原料的利用率高,方案二的实验中,发现容器底部残留少量紫红色固体,为铜,不溶于稀硫酸;
故答案为:不产生污染空气的SO2气体,制取等量的CuSO4溶液,消耗的硫酸量少;Cu;
方案二:(1)方案三的实验流程如图1中,双氧水反应氧化还原反应生成O2;随着反应的进行,生成气体速度加快,可能是反应产生的Cu2+对H2O2分解有催化作用,
故答案为:O2;反应产生的Cu2+对H2O2分解有催化作用;
(2)取H2O2溶液,向其中滴加CuSO4溶液,如果产生气泡的速率加快,则证明Cu2+对H2O2分解有催化作用,否则,Cu2+对H2O2分解没有催化作用;
故答案为:取H2O2溶液,向其中滴加CuSO4溶液,观察产生气泡的速率是否加快;
(3)根据离子方程式,3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,反应消耗2mol硝酸,生成3mol硫酸铜,故为了得到较纯净的硫酸铜溶液,硫酸和硝酸的物质的量之比应为3:2,故答案为:3:2;
(4)设计实验方案时,为防止NO污染空气,应通入空气氧化NO为NO2,用水吸收后,生成HNO3再循环利用,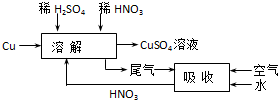 ,故答案为:
,故答案为: .
.
点评 此题难度较大,依据题目的要求结合反应原理分析即可;分析一个反应的可行性要从多方面分析,如从反应的可行性,环保安全,操作简便,经济节能方面考虑.


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:选择题
| A. | 其他条件不变,减小容器体积,平衡不移动 | |
| B. | 其他条件不变,增大c(A),A的转化率增大 | |
| C. | 降低温度,v正增大,v逆减小 | |
| D. | v正(A)═2v逆(C) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅥⅠA | 0 | |
| 2 | ⑥ | ⑦ | ⑪ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
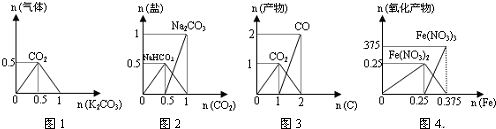
| A. | 图1:n (HCl)=1 mol,K2CO3逐步加入到HCl溶液中,在敞口容器中生成的气体 | |
| B. | 图2:n (NaOH)=1 mol,CO2逐步通入到NaOH溶液中反应生成的盐 | |
| C. | 图3:n (O2)=1 mol,高温下C和O2在密闭容器中的反应产物 | |
| D. | 图4:n (HNO3)=1 mol,Fe和稀HNO3反应生成的氧化产物(还原产物为NO) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2 L SO3中含有0.5NA个SO3分子 | |
| B. | 48g O3气体含有3NA个氧原子 | |
| C. | 在1L0.5mol•L-lFeCl3溶液中含有0.5NA个Fe3+ | |
| D. | 1.5 mol NO2与足量水反应,转移的电子数为1.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稳定性:PH3>H2S>HCl | B. | 酸性:HClO4>HBrO4>HIO4 | ||
| C. | 非金属性:F>O>S | D. | 碱性:NaOH>Mg(OH)2>Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锥形瓶 | B. | 试管 | C. | 分液漏斗 | D. | 250mL容量瓶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com