
如右图所示,常温下电解5 min后,铜电极质量增加2.16g。
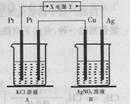 试回答:
试回答:
(l)电源电极X名称为_______(填“正极”或“负极”)。
(2)电解池B中阴极的电极反应式是__________。
(3)若A中KCl溶液的体积是200mL,电解后溶液的
pH=_________(忽略电解前后溶液体积的变化)。
若要使电解后的溶液恢复到与电解完完全相同,应加入的物质是__________。
(4)已知在l0lkPa时,CO的燃烧热为283 kJ/mol。相同条件下,若2 molCH4完全燃烧生成液态水,所放出的热量为1 mol CO完全燃烧放出热量的6.30倍,则CH4完全燃烧的热化学方程式为__________。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.海水淡化可以解决淡水供应危机,向海水中加入明矾可以使海水淡化
B.我国自行研制的“神七”航天服是由新型“连续纤维增韧”材料做成的,其主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料
C.“地沟油”危害健康,不仅是因为人体所必需的维生素E及脂肪酸油脂已经被破坏,营养低,而且含有黄曲霉素、苯并芘,这两种毒素都是致癌物
D.纸层析法、钠熔法、铜丝燃烧法都是定性分析法
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)有下列八种物质:①MgCl2晶体 ②干冰 ③NaOH晶体 ④白磷(P4)晶体 ⑤金刚石 ⑥硼晶体,其中属于离子晶体的是 ;属于分子晶体的是 ,属于原子晶体的是___ _。
(2)SO2的分子构型为 ,请从分子构型的角度分析SO2、CO2在水中溶解度的差别
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中能大量共存的是
A.pH=1的溶液中:
B.由水电离的c (H+)=1 x10
 的溶液中:
的溶液中:
C.c (Fe3+)=0.1 mol 的溶液中:
的溶液中: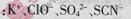
D.c (H+)/c (OH-)=10的溶液中:
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组进行电化学实验,研究装置如图所示。
有关说法不正确的是
A.镁为负极
B.原电池中碳极的电极反应式为
C.电解池中阳极处先变红
D.电解池中阴极的电极反应式为

查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)放热反应不需要加热就能反应,吸热反应不加热就不能反应 ( )
(2)物质发生化学变化都伴有能量的变化 ( )
(3)伴有能量变化的物质变化都是化学变化 ( )
(4)吸热反应在任何条件都不能发生 ( )
(5)Na转化为Na+时,吸收的能量就是该过程的反应热 ( )
(6)水蒸气变为液态水时放出的能量就是该变化的反应热 ( )
(7)同温同压下,反应H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH不同( )
(8)可逆反应的ΔH表示完全反应时的热量变化,与反应是否可逆无关 ( )
查看答案和解析>>
科目:高中化学 来源: 题型:
在298 K、101 kPa时,充分燃烧一定量的丁烷,放出热量Q kJ(Q>0),经测定完全吸收生成的二氧化碳需要消耗5 mol·L-1的KOH溶液100 mL,恰好生成正盐。则此条件下,下列热化学方程式正确的是 ( )
A.C4H10(g)+ O2(g)===4CO2(g)+5H2O(l)
O2(g)===4CO2(g)+5H2O(l)
ΔH=-16Q kJ·mol-1
B.C4H10(g)+ O2(g)===4CO2(g)+5H2O(l)
O2(g)===4CO2(g)+5H2O(l)
ΔH=-8Q kJ·mol-1
C.C4H10(g)+ O2(g)===4CO2(g)+5H2O(l)
O2(g)===4CO2(g)+5H2O(l)
ΔH=-Q kJ·mol-1
D.C4H10(g)+ O2(g)===4CO2(g)+5H2O(g)
O2(g)===4CO2(g)+5H2O(g)
ΔH=-Q kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
完成下列小题。
(1)[2013·江苏,20(1)]白磷(P4)可由Ca3(PO4)2、焦炭和SiO2在一定条件下反应获得。相关热化学方程式如下:
2Ca3(PO4)2(s)+10C(s)===6CaO(s)+P4(s)+10CO(g) ΔH1=+3 359.26 kJ·mol-1
CaO(s)+SiO2(s)===CaSiO3(s) ΔH2=-89.61 kJ·mol-1
2Ca3(PO4)2(s)+6SiO2(s)+10C(s)===6CaSiO3(s)+P4(s)+10CO(g) ΔH3
则ΔH3=________kJ·mol-1。
(2)[2013·四川理综,11(5)节选]焙烧产生的SO2可用于制硫酸。已知25 ℃、101 kPa时:
2SO2(g)+O2(g)2SO3(g) ΔH1=-197 kJ·mol-1;
H2O(g)===H2O(l) ΔH2=-44 kJ·mol-1;
2SO2(g)+O2(g)+2H2O(g)===2H2SO4(l)
ΔH3=-545 kJ·mol-1。
则SO3(g)与H2O(l)反应的热化学方程式是________。
(3)[2013·浙江理综,27(1)]捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应:
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g)(NH4)2CO3(aq)ΔH1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g)NH4HCO3(aq)ΔH2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g)2NH4HCO3(aq)ΔH3
ΔH3与ΔH1、ΔH2之间的关系是:ΔH3=________。
(4)[2013·天津理综,10(2)①]为减少SO2的排放,常采取的措施有:
将煤转化为清洁气体燃料。
已知:H2(g)+ O2(g)===H2O(g)
O2(g)===H2O(g)
ΔH=-241.8 kJ·mol-1
C(s)+ O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
O2(g)===CO(g) ΔH=-110.5 kJ·mol-1
写出焦炭与水蒸气反应的热化学方程式:____________________________________。
(5)[2013·北京理综,26(2)①]汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:
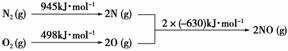
写出该反应的热化学方程式:_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
以下的说法正确的是( )
A、通式为C n H2n+2的有机物一定属于烷烃
B、通式为C n H2n的有机物一定属于烯烃
C、通式为C n H2n-2的有机物一定属于炔烃
D、通式为C n H2n-6(n≥6)的有机物一定属于芳香烃
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com