
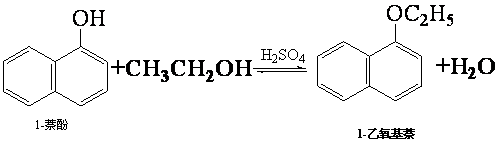
| 物质 | 相对分 子质量 | 状态 | 熔点(℃) | 沸点(℃) | 溶解度 | |
| 水 | 乙醇 | |||||
| 1-萘酚 | 144 | 无色或黄色菱形结晶或粉末 | 96℃ | 278℃ | 微溶于水 | 易溶于乙醇 |
| 1-乙氧基萘 | 172 | 无色液体 | 5.5℃ | 267℃ | 不溶于水 | 易溶于乙醇 |
| 乙醇 | 46 | 无色液体 | -114.1℃ | 78.5℃ | 任意比混溶 | |
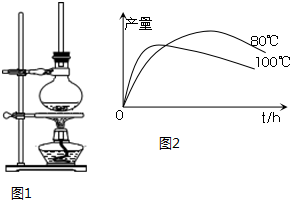
分析 (1)该反应中乙醇的量越多,越促进1-萘酚转化;
(2)长玻璃管起到冷凝回流的作用,提高乙醇原料的利用率;
(3)该产物沸点高于乙醇,从而降低反应物利用率;
(4)提纯产物用10%的NaOH溶液碱洗并分液,把硫酸洗涤去,水洗并分液洗去氢氧化钠,用无水氯化钙干燥并过滤,吸收水,控制沸点通过蒸馏的方法得到;
(5)时间延长、温度升高,1-乙氧基萘的产量下降的原因可能是酚羟基被氧化,乙醇大量挥发或产生副反应等;
(6)根据方程式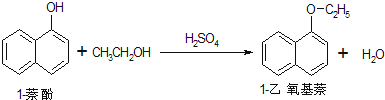 知,1-萘酚与1-乙氧基萘的物质的量相等,则n(C10H8O)=n(C12H12O)=$\frac{72g}{144g/mol}$=0.5mol,则m(C12H12O)=0.5mol×172g/mol=86g,据此计算其产率.
知,1-萘酚与1-乙氧基萘的物质的量相等,则n(C10H8O)=n(C12H12O)=$\frac{72g}{144g/mol}$=0.5mol,则m(C12H12O)=0.5mol×172g/mol=86g,据此计算其产率.
解答 解:(1)该反应中乙醇的量越多,越促进1-萘酚转化,从而提高1-萘酚的转化率,故答案为:提高1-萘酚的转化率;
(2)长玻璃管起到冷凝回流的作用,使挥发出的乙醇冷却后回流到烧瓶中,从而提高乙醇原料的利用率,故答案为:冷凝回流;
(3)该产物沸点高于乙醇,从而降低反应物利用率,所以不能用制取乙酸乙酯的装置,
故答案为:不能,产物沸点大大高于反应物乙醇,会降低产率;
(4)提纯产物用10%的NaOH溶液碱洗并分液,把硫酸洗涤去,水洗并分液洗去氢氧化钠,用无水氯化钙干燥并过滤,吸收水,控制沸点通过蒸馏的方法得到,实验的操作顺序为:③②④①;
故答案为:a;
(5)时间延长、温度升高,可能是酚羟基被氧化,乙醇大量挥发或产生副反应等,从而导致其产量下降,
故答案为:1-萘酚被氧化;温度高乙醇大量挥发或温度高发生副反应;
(6)根据方程式 知,1-萘酚与1-乙氧基萘的物质的量相等,则n(C10H8O)=n(C12H12O)=$\frac{72g}{144g/mol}$=0.5mol,则m(C12H12O)=0.5mol×172g/mol=86g,其产率=$\frac{43g}{86g}$×100%=50%,
知,1-萘酚与1-乙氧基萘的物质的量相等,则n(C10H8O)=n(C12H12O)=$\frac{72g}{144g/mol}$=0.5mol,则m(C12H12O)=0.5mol×172g/mol=86g,其产率=$\frac{43g}{86g}$×100%=50%,
故答案为:50%.
点评 本题考查有机物制备,为高频考点,明确实验原理及物质性质是解本题关键,对于有机反应大多数学生较陌生,以乙酸乙酯的制取为载体分析解答该实验,熟练掌握实验基本操作及物质分离和提纯方法,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | $\frac{m}{32}$ mol-1 | B. | 16m mol-1 | C. | m mol-1 | D. | 32m mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 元素编号 | 元素性质或原子结构 |
| T | 失去一个电子后,形成Ne原子电子层结构 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 其单质之一是空气中主要成分,最常见的助燃剂 |
| Z | 形成双原子单质分子,黄绿色气体 |
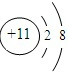 .
.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 用1g 98%的浓硫酸加入4g水配制1:4硫酸溶液 | |
| B. | 配制2.0mo1•L-1硫酸溶液时,最后在容量瓶中加水稀释到标线,塞好盖子倒转摇匀后,发现液面低于标线 | |
| C. | 在100mL无水乙醇中,加人2g甲醛配制2%的甲醛洒精溶液 | |
| D. | 在80mL水中,加入18.4mol•L-1浓硫酸20mL,配制3.68mol•L-1稀硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
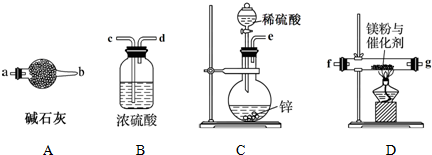
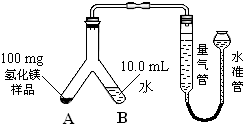
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 乙醇 | 溴乙烷 | 溴 | |
| 状态 | 无色液体 | 无色液体 | 深红棕色液体 |
| 密度/g•cm-3 | 0.79 | 1.44 | 3.1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
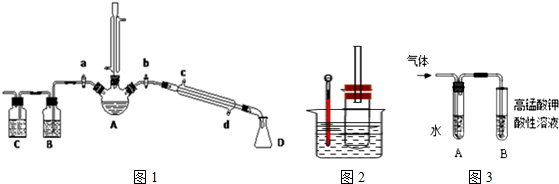
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 甘氨酸(NH2CH2COOH) | 柠檬酸 | 甘氨酸亚铁 |
| 易溶于水,微溶于乙醇,两性化合物 | 易溶于水和乙醇,有较强酸性和还原性 | 易溶于水,难溶于乙醇 |
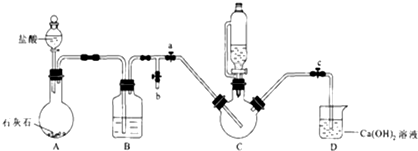
| 实验 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| 体系pH | 4.0 | 4.5 | 5.0 | 5.5 | 6.0 | 6.5 | 7.0 | 7.5 |
| 产率/% | 65.74 | 74.96 | 78.78 | 83.13 | 85.57 | 72.98 | 62.31 | 56.86 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 少量SO2通入NaClO溶液中:SO2+3ClO-+H2O═SO42-+Cl-+2HClO | |
| B. | 等物质的量的MgCl2、Ba(OH)2 和HCl溶液混合:Mg2++2OH-═Mg(OH)2↓ | |
| C. | 用硫氰化钾溶液可以检验溶液中的Fe3+:Fe3++3SCN-═Fe(SCN)3↓ | |
| D. | (NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制 Fe(OH)2:Fe2++2OH-═Fe(OH)2↓ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com