
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
|
| A. | 7.8 g苯中含有0.3NA个碳碳双键,0.3NA个碳碳单键 |
|
| B. | 5.6 g铁与足量的稀硝酸反应,失去电子数为0.2NA |
|
| C. | 32g硫(结构见图)含S﹣S的数目为NA
|
|
| D. | 含0.2 mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1 NA |
考点:
阿伏加德罗常数.
专题:
阿伏加德罗常数和阿伏加德罗定律.
分析:
A.苯分子中的碳碳键为一种介于单键和双键之间的独特键,苯分子中不存在碳碳双键;
B.铁与足量稀硝酸反应生成的是铁离子,5.6g铁的物质的量为: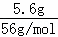 =0.1mol,0.1molFe与足量稀硝酸完全反应失去0.3mol电子;
=0.1mol,0.1molFe与足量稀硝酸完全反应失去0.3mol电子;
C.根据图示硫原子的结构简式可知,每个S原子形成了2个S﹣S键,根据均摊法计算出32g硫原子形成的共价键数目;
D.铜与浓硫酸的反应中,随着反应的进行,浓硫酸变成稀硫酸,反应停止,所以反应生成的二氧化硫的物质的量小于0.1mol.
解答:
解:A.7.8g苯的物质的量为: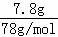 =0.1mol,苯分子中的碳碳键为一种独特键,其分子中不存在碳碳双键,故A错误;
=0.1mol,苯分子中的碳碳键为一种独特键,其分子中不存在碳碳双键,故A错误;
B.5.6g铁的物质的量为: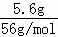 =0.1mol,0.1molFe与足量稀硝酸完全反应失去0.3mol电子,失去电子数为0.3NA,故B错误;
=0.1mol,0.1molFe与足量稀硝酸完全反应失去0.3mol电子,失去电子数为0.3NA,故B错误;
C.32g硫的物质的量为: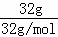 =1mol,根据图示结构简式可知,每个S原子与其它两个S形成两个S﹣S键,平均每个硫原子形成的共价键数目为:
=1mol,根据图示结构简式可知,每个S原子与其它两个S形成两个S﹣S键,平均每个硫原子形成的共价键数目为: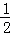 ×2=1,所以1molS原子形成的S﹣S共价键的物质的量为1mol,含S﹣S的数目为NA,故C正确;
×2=1,所以1molS原子形成的S﹣S共价键的物质的量为1mol,含S﹣S的数目为NA,故C正确;
D.如果0.2 mol H2SO4的浓硫酸与足量铜完全反应,则会生成0.1mol二氧化硫气体,由于随着反应的进行,浓硫酸变成稀硫酸,反应停止,所以该反应中生成二氧化硫的物质的量小于0.1mol,生成SO2的分子数小于0.1 NA,故D错误;
故选C.
点评:
本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确苯分子中碳碳键特点,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项C为难点、易错点,注意均摊法的应用.


科目:高中化学 来源: 题型:
欲配制100mL 1.0mol/L Na2SO4溶液,正确的方法是( )
①将14.2g Na2SO4溶于100ml水中
②将32.2g Na2SO4•10H2O溶于少量水中,再用水稀释至100ml
③将20mL 5.0mol/L Na2SO4溶液用水稀释至100ml.
A. ①② B. ②③ C. ①③ D. ①②③
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液中,跟100mL 0.5mol/L NaCl溶液所含的Cl﹣物质的量浓度相同的是( )
|
| A. | 100mL 0.5mol/L MgCl2溶液 |
|
| B. | 200mL 0.25mol/L CaCl2溶液 |
|
| C. | 50ml 1mol/L NaCl溶液 |
|
| D. | 25ml 2mol/L HCl溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图是硫酸试剂瓶标签上的内容:
(1).则该硫酸的物质的量浓度为 mol•L﹣1.
(2).某化学兴趣小组进行硫酸性质的实验探究时,需要240mL 4.6mol•L﹣1的稀H2SO4,现取上述浓硫酸稀释配制稀硫酸,则所需实验仪器有 ,所需量取 mL的该硫酸.
(3)下面是某学生的操作过程:
a.将浓硫酸倒入另一个盛有适量蒸馏水的烧杯中稀释,并冷却到室温;
b.用量筒量取浓硫酸;
c.用玻璃棒引流,将稀释后的硫酸倒入已检查不漏水的容量瓶中;
d.将所得溶液倒入试剂瓶,在试剂瓶上贴上标签待用.
e.用胶头滴管加水至凹液面底部与刻度线相切,摇匀;
f.轻轻摇动容量瓶,使瓶内液体混合均匀,再向容量瓶中加水至离刻度线1cm~2cm
g.洗涤烧杯和玻璃棒,并将洗涤液注入容量瓶.
正确的操作顺序是 .(用字母表示)
(4)在配制4.6mol•L﹣1的稀H2SO4的过程中,下列情况对硫酸溶液物质的量浓度有何影响(填“偏高”“偏低”或“无影响”)
①未经冷却趁热将溶液注入容量瓶中: ;
②容量瓶用1mol•L﹣1的稀H2SO4润洗: ;
③定容时仰视液面读数: .
④容量瓶有蒸馏水 .

查看答案和解析>>
科目:高中化学 来源: 题型:
下面是生产生活中的常见有机物的分子式、结构式、结构简式或名称有关说法正确的是( )
① ②
②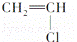 ③
③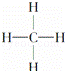 ④
④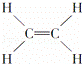 ⑤CH3CH2OH⑥C6H12O6⑦CH3COOH
⑤CH3CH2OH⑥C6H12O6⑦CH3COOH
⑧硬脂酸甘油酯、⑨蛋白质、⑩聚乙烯.
|
| A. | 能跟溴的四氯化碳溶液发生加成反应并使之褪色的有①②④⑩ |
|
| B. | 投入钠能产生H2的是⑤⑦⑧⑨ |
|
| C. | 属于高分子材料的是⑧⑨⑩ |
|
| D. | 含碳量最高、有毒、常温下为液体且点燃时有浓烟的是① |
查看答案和解析>>
科目:高中化学 来源: 题型:
新鲜水果、蔬菜、乳制品中富含的维生素C具有明显的抗衰老作用,但易被空气氧化.某课外小组利用碘滴定法测某橙汁中维生素C的含量,其化学方程式如下:
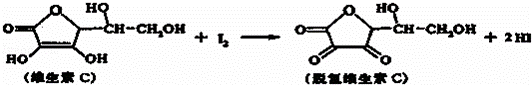
下列说法正确的是( )
|
| A. | 维生素C的分子式为C6H8O6 |
|
| B. | 维生素C在酸性条件下水解得到3种产物 |
|
| C. | 维生素C不溶于水,可溶于有机溶剂 |
|
| D. | 上述反应为取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关元素及其化合物性质的比较正确的是( )
|
| A. | 原子半径:F<O<Al | B. | 稳定性:H2O<PH3<NH3 |
|
| C. | 酸性:H2CO3<H2SO4<H3PO4 | D. | 碱性:LiOH<NaOH<Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
)下列溶液中微粒的物质的量浓度关系正确的是( )
|
| A. | Ca(ClO)2溶液中:c(Ca2+)>c(ClO﹣)>c(OH﹣)>c(H+) |
|
| B. | 等体积、等物质的量浓度的NaX和弱酸HX混合:c(Na+)=c(X﹣)>c(OH﹣)=c(H+) |
|
| C. | 常温下,将25mL0.2mol/L的盐酸与100mL0.1mol/L的氨水混合,所得溶液中:c(NH4+)>c(Cl﹣)>c(NH3•H2O)>c(OH﹣)>c(H+) |
|
| D. | 将0.1mol/L的Na2S溶液与0.1mol/L的NaHS溶液等体积混合,所得溶液中:c(S2﹣)+2c(OH﹣)=2c(H+)+c(HS﹣)+3c(H2S) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com