
| A. | 硫酸工业中,三氧化硫在吸收塔内被水吸收制成浓硫酸 | |
| B. | 炼铁工业中,用焦炭和空气反应产生的一氧化碳在高温下还原铁矿石中的铁 | |
| C. | 合成氨工业中,用铁触媒作催化剂,可提高单位时间氨的产量 | |
| D. | 氯碱工业中,电解槽的阴极区产生NaOH |
分析 A.吸收塔中SO3如果用水吸收,发生反应:SO3+H2O═H2SO4,该反应为放热反应,放出的热量易导致酸雾形成,阻隔在三氧化硫和水之间,阻碍水对三氧化硫的吸收;而浓硫酸的沸点高,难以气化,不会形成酸雾,同时三氧化硫易溶于浓硫酸;
B、工业制铁是CO还原铁矿石来制取;
C.催化剂不会引起化学平衡的移动,但是加快了化学反应速率,从而提高单位时间氨的产量;
D.电解池中和电源的负极相连的是电解池的阴极,阳离子得到电子发生还原反应;
解答 解:A.吸收塔中SO3如果用水吸收,发生反应:SO3+H2O═H2SO4,该反应为放热反应,放出的热量易导致酸雾形成,阻隔在三氧化硫和水之间,阻碍水对三氧化硫的吸收;而浓硫酸的沸点高,难以气化,不会形成酸雾,同时三氧化硫易溶于浓硫酸,所以工业上从吸收塔顶部喷洒浓硫酸作吸收液,最终得到“发烟”硫酸,故A错误;
B、工业制铁是CO还原铁矿石:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$ 2Fe+3CO2,故B正确;
C.催化剂不会引起化学平衡的移动,但是加快了化学反应速率,从而提高单位时间氨的产量,故C正确;
D.阴极是氢离子得到电子生成氢气发生还原反应,阴极附近水电离平衡破坏,氢氧根离子浓度增大结合钠离子生成氢氧化钠,故D正确;
故选A.
点评 本题考查反应原理,解答时须理解相关的化学反应发生的条件,平时应注意相关知识的积累,题目难度不大.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:多选题
| A. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g);△H=-1367.0 kJ/mol(燃烧热) | |
| B. | NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H=-57.3kJ/mol(中和热) | |
| C. | S(s)+$\frac{3}{2}$O2(g)═SO3(g);△H=-269.8kJ/mol(反应热) | |
| D. | 2NO2=O2+2NO;△H=+116.2kJ/mol(反应热) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ② | D. | ⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气体甲可与Z的某种氢化物反应生成强酸 | |
| B. | W元素的晶体单质是一种良好的半导体材料 | |
| C. | 化合物乙中一定只有共价键 | |
| D. | X分别与Y、Z、M、W形成的常见化合物中,稳定性最好的是XM |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
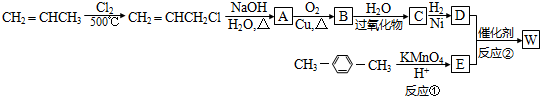
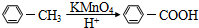
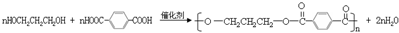 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2无毒,对大气不造成污染,所以可以无限量排放 | |
| B. | NaHCO3比Na2CO3稳定 | |
| C. | Na2CO3溶液可与Ba(OH)2溶液反应,NaHCO3溶液不与Ba(OH)2溶液反应 | |
| D. | NaHCO3溶液与NaOH溶液混合会发生反应,但观察不到明显的现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③④⑤ | C. | ①④⑤⑥ | D. | ①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 属于放热反应 | B. | 属于氧化还原反应 | ||
| C. | 由热能转化为化学能 | D. | 可用于工业生产熟石灰 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 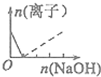 | B. | 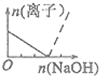 | C. | 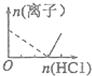 | D. | 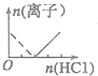 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com