
【题目】“封管实验”具有简易、方便、节约、绿色等优点,下列关于四个“封管实验”(夹持装置未画出)的说法正确的是( )

A.加热时,①中上部汇集了 NH4Cl 固体,说明 NH4Cl 的热稳定性比较好
B.加热时,②中溶液变红,冷却后又都变为无色
C.加热时,③中溶液变红,冷却后红色褪去,体现了 SO2 的漂白性
D.加热时,④中上部聚集了固体碘,说明碘的热稳定性较差
科目:高中化学 来源: 题型:
【题目】有机物X是一种烷烃,是液化石油气的主要成分,可通过工艺Ⅰ的两种途径转化为A和B、C和D。B是一种重要的有机化工原料,E分子中含环状结构,F中含有两个相同的官能团,D是常见有机物中含氢量最高的,H能使![]() 溶液产生气泡,Ⅰ是一种有浓郁香味的油状液体。
溶液产生气泡,Ⅰ是一种有浓郁香味的油状液体。
请回答:
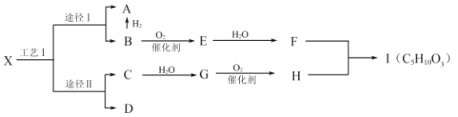
(1)G的结构简式为_________________________。
(2)G→H的反应类型是_________________________。
(3)写出F+H→1的化学方程式_________________________。
(4)下列说法正确的是_______。
A.工艺Ⅰ是石油的裂化
B.除去A中的少量B杂质,可在一定条件下往混合物中通入适量的氢气
C.X、A、D互为同系物,F和甘油也互为同系物
D.H与![]() 互为同分异构体
互为同分异构体
E.等物质的量的Ⅰ和B完全燃烧,消耗氧气的质量比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列![]() 种与人们生产生活相关的有机物:
种与人们生产生活相关的有机物:
①![]() (基础化工原料)②
(基础化工原料)②![]() (防霉剂)③
(防霉剂)③![]() (打火机燃料)④
(打火机燃料)④![]() (冷冻剂)⑤
(冷冻剂)⑤![]() (汽车防冻液)⑥
(汽车防冻液)⑥![]() (杀菌剂)
(杀菌剂)
请回答:
(1)属于醇的是________(填序号)。
(2)与①互为同系物的是________(填序号)。
(3)与③互为同分异构体的是________(填序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H是合成治疗心血管疾病药物的中间体,可通过以下途径合成:
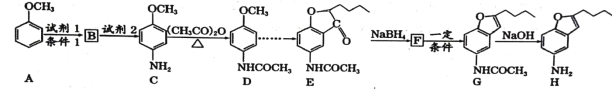
已知:①![]() (苯胺易被氧化)
(苯胺易被氧化)
②甲苯发生一硝基取代反应与A类似。
回答下列问题:
(1)写出化合物H的分子式__________,C中含氧官能团的名称___________。
(2)写出有关反应类型:B![]() C ___________;F
C ___________;F![]() G___________。
G___________。
(3)写出A![]() B的反应方程式:___________________________ 。
B的反应方程式:___________________________ 。
(4)写出同时满足下列条件D的所有同分异构体的结构简式:____________
①能发生银镜反应
②能发生水解反应,水解产物之一与FeCl3溶液反应显紫色
③核磁共振氢谱(1![]() 显示分子中有4种不同化学环境的氢
显示分子中有4种不同化学环境的氢
(5)合成途径中,C转化为D的目的是_____________________。
(6)参照上述合成路线,以甲苯和(CH3CO)2O为原料(无机试剂任选),设计制备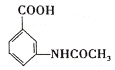 的合成路线:_________________________
的合成路线:_________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有8种物质:①甲烷 ②苯 ③聚乙烯 ④聚异戊二烯(![]() ) ⑤2-丁炔 ⑥环乙烷 ⑦邻二甲苯 ⑧2-甲基-1,3-丁二烯,既能使酸性高锰酸钾溶液褪色,又能与溴水反应使之褪色的是
) ⑤2-丁炔 ⑥环乙烷 ⑦邻二甲苯 ⑧2-甲基-1,3-丁二烯,既能使酸性高锰酸钾溶液褪色,又能与溴水反应使之褪色的是
A. ③④⑤⑧ B. ④⑤⑦⑧ C. ④⑤⑧ D. ③④⑤⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数。已知C2H4和C3H6的混合物的质量为a g,则该混合物( )
A.所含共用电子对数目为(a/7+1) NAB.所含原子总数为aNA/14
C.燃烧时消耗的O2一定是33.6 a/14LD.所含碳氢键数目为aNA/7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩种元素,请用化学用语回答下列问题:
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
2 | ⑥ | ⑦ | ⑧ | |||||
3 | ① | ③ | ⑤ | ⑨ | ⑩ | |||
4 | ② | ④ |
(1)在③~⑦元素中,原子半径最大的是__________(填元素符号);
(2)⑦元素的最高价氧化物对应的水化物与其氢化物能生成盐M,M中含有的化学键类型有__________________;
(3)写出元素①和⑧的单质在加热条件下反应生成的化合物的电子式:_________。
(4
(5)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是_____________(填物质化学式);呈两性的氢氧化物是_________(填物质化学式),该化合物与NaOH溶液反应的离子方程式为___________。
(6)用电子式表示元素③与⑨形成化合物的过程_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在固定容积为1.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g)![]() 2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
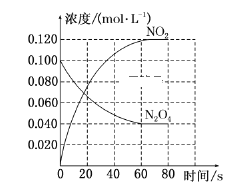
(1)反应的ΔH________(填“大于”或“小于”)0;100 ℃时,体系中各物质浓度随时间变化如上图所示。在0~60 s时段,反应速率v(N2O4)为______________________________。
(2)100 ℃时达到平衡后,改变反应温度为T,c(N2O4)降低,经10 s又达到平衡。
①T________(填“大于”或“小于”)100 ℃,判断理由是_____________________;
②100 ℃时达到平衡后,向容器中再充入0.20 mol NO2气体,新平衡建立后,NO2的体积分数________(填“增大”“不变”或“减小”)。
(3)温度T时反应达平衡后,将反应容器的容积减小一半,平衡向________(填“正反应”或“逆反应”)方向移动,判断理由是_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有AlCl3和MgSO4混合溶液,向其中不断加入NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为 ( )

A.1:3B.2:3
C.6:1D.3:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com