
| A. | 9.8g | B. | 15.3g | C. | 19.6g | D. | 30.6g |
分析 n(CuSO4•5H2O)=$\frac{25g}{250g/mol}$=0.1mol,根据Cu原子守恒得n(CuSO4•5H2O)=n(CuSO4),Cu和浓硫酸反应方程式为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,根据硫酸铜和被还原硫酸的关系式计算.
解答 解:n(CuSO4•5H2O)=$\frac{25g}{250g/mol}$=0.1mol,根据Cu原子守恒得n(CuSO4•5H2O)=n(CuSO4),Cu和浓硫酸反应方程式为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O,根据方程式知,该反应中有一半的硫酸做氧化剂,所以0.1mol硫酸铜生成时有0.1mol硫酸被还原,其质量=0.1mol×98g/mol=9.8g,故选A.
点评 本题以浓硫酸为载体考查氧化还原反应的计算,侧重考查分析计算能力,利用原子守恒及方程式进行计算,知道硫酸的作用,题目难度不大.


科目:高中化学 来源: 题型:解答题
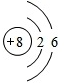 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2Na+2H2O═2NaOH+H2↑ | B. | CaO+H2O═Ca(OH)2 | ||
| C. | 3NO2+H2O═2HNO3+NO | D. | 2F2+2H2O═4HF+O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2:1:2 | B. | 5:5:4 | C. | 1:1:1 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | X是NH3,Y是KCl溶液 | B. | X是SO2,Y是NaOH | ||
| C. | X是H2,Y是浓硫酸 | D. | X是CO2,Y是KOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ③②④⑤① | C. | ④②③⑤① | D. | ③④②⑤① |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=2的硫酸 | B. | 0.01 mol•L-1的甲酸 | ||
| C. | pH=2的醋酸 | D. | 0.01 mol•L-1的硝酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com