
| A. | 元素B的单质与化合物A2D反应能生成D的单质 | |
| B. | 工业上利用铝热反应可制得单质C | |
| C. | 原子B、C、D半径的大小顺序:D>C>B | |
| D. | 一定条件下,过量的B单质与D单质直接生成BD3 |
分析 A、B、C、D是原子序数依次增大的短周期主族元素,A是周期表中原子半径最小的元素,则A为H元素;B原子最外层电子数是电子层数的3倍,可推知B为O元素;D与B属于同一主族,则D为S元素;CA2是一种储氢材料,C为+2价,而且原子序数大于O小于S,则C为Mg元素;结合元素周期律与元素化合物性质解答.
解答 解:A、B、C、D是原子序数依次增大的短周期主族元素,A是周期表中原子半径最小的元素,则A为H元素;B原子最外层电子数是电子层数的3倍,可推知B为O元素;D与B属于同一主族,则D为S元素;CA2是一种储氢材料,C为+2价,而且原子序数大于O小于S,则C为Mg元素;
A.氧气具有氧化性、硫化氢具有还原性,则元素O的单质与化合物H2S反应能生成S的单质,故A正确;
B.C为Mg,Mg的还原性大于Al,所以不能用铝热反应可制得单质Mg,故B错误;
C.电子层越多,原子半径越大,同周期随原子序数增大原子半径减小,故原子半径Mg>S>O,即半径的大小顺序:C>D>B,故C错误;
D.D为S元素,B为O元素,S在氧气中燃烧生成SO2,故D错误,
故选A.
点评 本题考查结构性质位置关系应用,根据原子结构和元素的性质推断元素是解题的关键,注意对元素周期律的理解掌握,题目难度不大.


 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
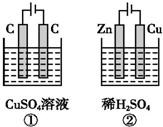 如图所示的两个实验装置中,溶液的体积均为 200mL,开始时电解质溶液的浓度均为 0.1mol•L-1,工作一段时间后,测得两端导线中均通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是( )
如图所示的两个实验装置中,溶液的体积均为 200mL,开始时电解质溶液的浓度均为 0.1mol•L-1,工作一段时间后,测得两端导线中均通过0.02mol电子,若不考虑盐的水解和溶液体积的变化,则下列叙述中正确的是( )| A. | 产生气体的总体积:①>② | |
| B. | 电极上析出物质的总质量:②>① | |
| C. | 溶液的pH变化:①增大,②减小 | |
| D. | ①中阳极的电极反应式:4OH--4e-═2H2O+O2↑;②中阴极的电极反应式:2H++2e-═H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=11的Na2SO3溶液中,水电离的c(H+)=1.0×10-11mol/L | |
| B. | 将0.2mol•L-1盐酸与0.1mol•L-1的KAlO2溶液等体积混合,溶液中离子浓度由小到大的顺序:c(OH-)<c(Al3+)<c(H+)<c(K+)<c(Cl-) | |
| C. | 浓度相同的①NH4Cl②(NH4)2SO4③(NH4)2CO3④NH4HSO4四种溶液,c(NH4+)大小顺序为:②>③>④>① | |
| D. | pH=4的NaHC2O4溶液中存在:c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+c(C2O42-) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol•L-1K2SO4溶液中含有K+的数目为2NA | |
| B. | 标准状况下,2.24L氯仿(CHCl3)中含有C-Cl数目为0.3NA | |
| C. | 18g重水中所含有的中子数为10NA | |
| D. | 1molNa与O2在一条条件下反应生成Na2O和Na2O2的混合物的转移电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,密度为dg/L的某气体纯净物一个分子的质量为22.4d/NAg | |
| B. | 加热条件下,20mL10mol/L的浓硝酸与足量铜反应转移电子数为0.1NA | |
| C. | 电解精炼铜的过程中转移了NA个电子,则阴极析出32g铜 | |
| D. | 1L pH=1的硫酸溶液中,含有0.1NA个H+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com