
【题目】由3种常见短周期元素组成的化合物A,相对分子质量为119,能与水剧烈反应,生成2种酸性气体的混合气体B。现对化合物A进行下列实验,假设各步反应均完全,反应中气体完全逸出。
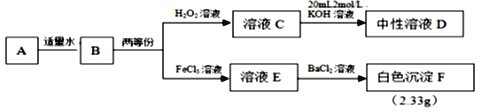
请回答:
(1)D中溶质的化学式_____________________,H2O2的电子式_______________。
(2)A和水反应的化学方程式___________________________________________。
(3)B→E的离子方程式______________________________________________。
【答案】 K2SO4、KCl ![]() SOCl2+H2O=SO2↑+2HCl↑ SO2+2Fe3+ +2H2O=2Fe2++SO42-+4H+
SOCl2+H2O=SO2↑+2HCl↑ SO2+2Fe3+ +2H2O=2Fe2++SO42-+4H+
【解析】由3种常见短周期元素组成的化合物A,相对分子质量为119,能与水剧烈反应,生成2种酸性气体的混合气体B。B中的气体能够与双氧水反应,说明含有一种具有还原性的气体,被双氧水氧化后的产物C与氢氧化钾溶液反应后显中性,说明C为强酸,则B中含有二氧化硫,C中含有硫酸;B与氯化铁溶液反应,B中的二氧化硫被氧化生成硫酸,与氯化钡反应生成硫酸钡沉淀,根据硫酸钡沉淀的质量,可以求出二氧化硫的物质的量=硫酸钡的物质的量=![]() =0.01mol;因为氢氧化钾为0.02L×2 mol/L=0.04mol,则B中还含有一种强酸性物质,且能与0.02mol氢氧化钾恰好反应;根据化合物A由3种常见短周期元素组成,相对分子质量为119,能与水剧烈反应,生成2种酸性气体的混合气体B,根据元素守恒,另一种酸性气体为氢化物,则另一种物质为HCl,因此A为SOCl2。
=0.01mol;因为氢氧化钾为0.02L×2 mol/L=0.04mol,则B中还含有一种强酸性物质,且能与0.02mol氢氧化钾恰好反应;根据化合物A由3种常见短周期元素组成,相对分子质量为119,能与水剧烈反应,生成2种酸性气体的混合气体B,根据元素守恒,另一种酸性气体为氢化物,则另一种物质为HCl,因此A为SOCl2。
(1)根据上述分析,D中溶质有硫酸钾和氯化钾,H2O2的电子式为![]() ,故答案为:K2SO4、KCl;
,故答案为:K2SO4、KCl;![]() ;
;
(2)A(SOCl2)和水反应的化学方程式为SOCl2+H2O=SO2↑+2HCl↑,故答案为:SOCl2+H2O=SO2↑+2HCl↑;
(3)B→E的过程中二氧化硫被氯化铁氧化,反应的离子方程式为SO2+2Fe3+ +2H2O=2Fe2++SO42-+4H+,故答案为:SO2+2Fe3+ +2H2O=2Fe2++SO42-+4H+。


 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】反应N2O4(g)2NO2(g)△H=+57kJmol﹣1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示.下列说法正确的是
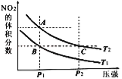
A. A、C两点的反应速率:A>C
B. A、C两点气体的颜色:A深,C浅
C. A、B两点气体的平均相对分子质量:A>B
D. B、C两点化学平衡常数:B<C
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某固体可能含有NH4+、Cu2+、Na+、Cl-、CO32-、SO42-中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离);
(1)一份固体溶于水得无色透明溶液,加入足量BaCl2溶液,得沉淀6.63g,在沉淀中加入过量稀盐酸,仍有4.66g沉淀。
(2)另一份固体与过量NaOH固体混合后充分加热,产生使湿润的红色石蕊试纸变蓝色的气体0.672L(标准状况)。
下列说法正确的是
A. 该固体中一定含有NH4+、CO32-、SO42-、Na+ B. 该固体中一定没有Cu2+、Cl-、Na+
C. 该固体中只含有NH4+、CO32-、SO42-、Cl- D. 根据以上实验,无法确定该固体中有Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氯化六氨合钴(Ⅲ)是一种重要的化工产品,实验中采用H2O2作氧化剂,在大量氨和氯化铵存在下,选择活性炭作为催化剂将Co(Ⅱ)氧化为Co(Ⅲ),来制备三氯化六氨合钴(Ⅲ)配合物,反应式为:2(CoCl2·6H2O)+10NH3+2NH4Cl+H2O2![]() 2[Co(NH3)6]Cl3+14H2O
2[Co(NH3)6]Cl3+14H2O

已知:①Co(NH3)6Cl3在不同温度下水中的溶解度曲线如图。
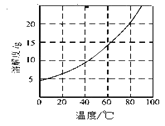
②制备过程中可能用到的部分装置如下:
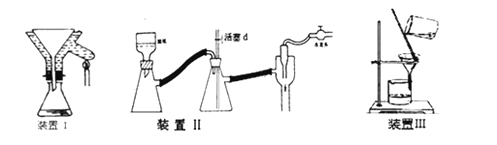
(1)原料NH4Cl的主要作用是_________;步骤④中要冷却至10℃再加入H2O2溶液,这样操作的目的:_____。
(2)步骤⑤中保持60℃的加热方法是_____,恒温20分钟的目的是_____。
(3)步骤⑥是减压抽滤(见上图装置Ⅱ),当抽滤完毕或中途停止抽滤时,防自来水倒吸入抽滤瓶最佳的正确操作是_____。
(4)操作A的名称为_____。若操作过程中,发现漏斗尖嘴处有少量晶体析出,处理方法是_________。
(5)步骤⑨进行洗涤时要用到两种试剂,应该依次用_____(填序号)洗涤。
A. 饱和氯化钠溶液 B. 无水乙醇 C. 浓盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】涤纶广泛应用于衣料和装饰材料。合成涤纶的反应如下:
![]()
下列说法正确的是
A. 合成涤纶的反应为加聚反应
B. 对苯二甲酸和苯甲酸互为同系物
C. 1 mol涤纶与NaOH溶液反应,理论上最多可消耗2n mol NaOH
D. 涤纶的结构简式为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质的分类、名称(或俗名)、化学式中不能完全对应的是( )
A.碱性氧化物、过氧化钠、Na2O2
B.酸性氧化物、三氧化硫、SO3
C.正盐、苏打、Na2CO3
D.含氧酸、次氯酸、HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳及其化合物广泛存在于自然界中,回答下列问题:
(1)在基态碳原子中,核外存在______对自旋相反的电子。
(2)碳是形成化合物种类最多的元素:常见的有机物CH3COOH中c原子轨道杂化类型为___________,乙酸中官能团的名称为__________________。
(3)碳元素的单质有多种形式,下图依次是C60、石墨和金刚石的结构图:

回答下列问题:
①金刚石、石墨烯(指单层石墨)中C-C键夹角大小为石墨烯________金刚石(填“>”或“<”)。
②已知金刚石里C-C键长为154pm,石墨里C-C键长为142 pm,C60、石墨、金刚石熔点从高到低的顺序为______________________;其中石墨与金刚石熔点高低顺序的原因为:_____________________________________________。
③一个金刚石晶胞含有_______个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r=_________a。
④石墨晶胞如图虚线所示,切出来的晶胞如图所示,则一个石墨晶胞含有碳原子个数为_________,已知石量的密度为ρg/cm3,层内的碳原子核向距为dcm,阿伏加德罗常数的值为NA,计算石墨晶体的层间距为_________cm。(C的相对原子质量为12)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com