
【题目】下列各项叙述中,正确的是( )
A.Ge的电负性为1.8,则其是典型的非金属
B.L层不含s能级,M层存在3f能级
C.焰火是焰色反应,都是电子由基态跃迁到激发态的结果
D.在电子云示意图中,小黑点是电子在原子核外出现的概率密度的形象描述
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A.用醋酸溶解大理石:CaCO3+2H+=Ca2++H2O+CO2↑
B.向氯化铝溶液中滴加过量氨水:Al3++4NH3?H2O=AlO ![]() +4NH+4+2H2O
+4NH+4+2H2O
C.向碳酸氢钙溶液中加入少量烧碱溶液:Ca2++2HCO ![]() +2OH﹣=CaCO3↓+CO
+2OH﹣=CaCO3↓+CO ![]() +H2O
+H2O
D.亚硫酸钠溶液中滴加酸性高锰酸钾溶液:5SO ![]() +6H++2MnO
+6H++2MnO ![]() =5SO
=5SO ![]() +2Mn2++3H2O
+2Mn2++3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用一张已除去表面氧化膜的铝箔紧紧包裹在试管外壁(如图),将试管浸入硝酸汞溶液中,片刻取出,然后置于空气中,不久铝箔表面生出“白毛”,红墨水柱右端上升.根据实验现象判断下列说法错误的是( ) 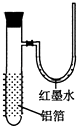
A.实验中发生的反应都是氧化还原反应
B.铝是一种较活泼的金属
C.铝与氧气反应放出大量的热量
D.铝片上生成的白毛是氧化铝和氧化汞的混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄钠铁矾[NaaFeb(SO4)c(OH)d]具有沉淀颗粒大、沉淀速率快、容易过滤等特点.某研究小组先将某废水中Fe2+氧化为Fe3+ , 再加入Na2SO4使其生成黄钠铁矾而除去铁.为测定黄钠铁矾的组成,该小组进行了如下实验:
①称取12.125g样品,加盐酸完全溶解后,配成250.00mL溶液A.
②量取25.00mL溶液A,加入足量的KI,再用0.2500molL﹣1Na2S2O3溶液滴定生成的I2(反应原理为I2+2Na2S2O3=2NaI+Na2S4O6),消耗30.00mL Na2S2O3溶液至终点.
③另取50.00mL溶液A,加入足量BaCl2溶液充分反应后,过滤,将所得沉淀洗涤、干燥后,称得其质量为2.330g.
(1)NaaFeb(SO4)c(OH)d中a、b、c、d之间的代数关系式为 .
(2)通过计算确定黄钠铁矾的化学式(写出计算过程).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种元素均位于周期表的前四周期,且原子序数依次增大.元素A是原子半径最小的元素;B元素基态原子的核外电子分占四个原子轨道(能级);D元素原子的已成对电子总数是未成对电子总数的3倍;E与D处于同一主族;F位于ds区,且原子的最外层只有1个电子.
(1)F+离子的电子排布式是 .
(2)B,C,D元素的第一电离能由大到小的顺序是 .
(3)B,C元素的某些氢化物的分子中均含有18个电子,则B的这种氢化物的化学式是;B、C的这些氢化物的沸点相差较大的主要原因是 .
(4)A,B,D可形成分子式为A2BD的某化合物,则该化合物分子中B原子的轨道杂化类型是;1mol该分子中含有π键的数目是 .
(5)C,F两元素形成的某化合物的晶胞结构如图所示,则该化合物的化学式是 , C原子的配位数是 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列选用的除杂试剂和实验操作都正确的是(括号内为杂质)( )
物质 | 除杂试剂(足量) | 操作方法 | |
A | CO2(HC1) | 氢氧化钠溶液 | 气体通过盛有氢氧化钠溶液的洗气瓶 |
B | K2CO3(KCl) | 稀盐酸 | 加入稀盐酸、蒸发、结晶 |
C | FeSO4(CuSO4) | 铁粉 | 加入铁粉并过滤 |
D | Zn(Fe) | 稀硫酸 | 加入稀硫酸,过滤 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铁的氧化物,用7mol/L的盐酸100mL在一定条件下恰好完全溶解,所得溶液再通入0.56L标准状况下的氯气时,刚好使溶液中Fe2+完全转化为Fe3+ . 则该氧化物的化学式可表示为( )
A.FeO
B.Fe3O4
C.Fe4O5
D.Fe5O7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列物质的说法,正确的是( ) 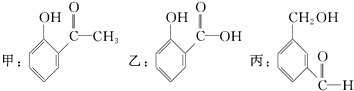
A.三者含有的官能团的种类相同
B.乙和丙中的﹣OH性质相同
C.甲和乙互为同分异构体
D.甲和丙互为同分异构体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com