

| A. | Y、Q两种元素的气态氢化物及其最高价氧化物的水化物均为强酸 | |
| B. | 最高价氧化物对应水化物的碱性:Z<M | |
| C. | 气态氢化物的稳定性:R>Q | |
| D. | 简单离子的半径:X>Z>M |
分析 由短周期元素原子半径与原子序数可知,X、Y为第二周期元素,Z、M、R、Q为第三周期元素,且非金属性Y>X,Q>R>M>Z,以此来解答.
解答 解:A.同周期从左向右原子半径减小、非金属性增强,非金属性Y>X,Q>R>M>Z,但Y可能为F,不存在最高价含氧酸,且HF为弱酸,故A错误;
B.同周期从左向右原子半径减小,金属性减弱,则金属性Z>M,最高价氧化物对应水化物的碱性:Z>M,故B错误;
C.非金属性Q>R,则气态氢化物的稳定性为Q>R,故C错误;
D.具有相同电子排布的离子中原子序数大的离子半径小,则简单离子的半径:X>Z>M,故D正确;
故选D.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素的位置、性质、元素周期律为解答的关键,侧重分析与应用能力的考查,注意金属性、非金属性的比较,题目难度不大.


科目:高中化学 来源: 题型:实验题
 如图所示装置可用来制取和观察Fe(OH)2在空气中被氧化时颜色的变化.实验时必须使用铁屑、4mol•L-1的硫酸溶液,其他试剂任选.填写下列空白.
如图所示装置可用来制取和观察Fe(OH)2在空气中被氧化时颜色的变化.实验时必须使用铁屑、4mol•L-1的硫酸溶液,其他试剂任选.填写下列空白.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4.4g由CO2和N2O组成的混合气体中的氧原子数为2.2NA | |
| B. | 12g由612C60和614C60组成的固体中的原子数为NA | |
| C. | 常温常压下,22.4LNH3中所含的共价键数为3NA | |
| D. | 1L1mol•L-1次氯酸溶液中的CIO-数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加大CaCO3的量 | B. | 加大盐酸的浓度 | C. | 加大盐酸的量 | D. | 减少CaCl2的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验编号 | 起始浓度/mol•L-1 | 反应后溶液的pH | |
| c(HA) | c(KOH) | ||
| ① | 0.1 | 0.1 | 9 |
| ② | X | 0.2 | 7 |
| A. | 实验①反应后的溶液中:c(K+)>c(A-)>c(OH-)>c(H+) | |
| B. | 实验①反应后的溶液中:c(OH-)=c(K+)-c(A-)=$\frac{{K}_{W}}{1×1{0}^{-5}}$mol•L-1 | |
| C. | 实验②反应后的溶液中:c(A-)+c(HA)>0.1mol•L-1 | |
| D. | 实验②反应后的溶液中:c(K+)=c(A-)>c(OH-)=c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
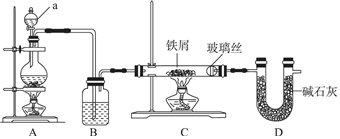
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
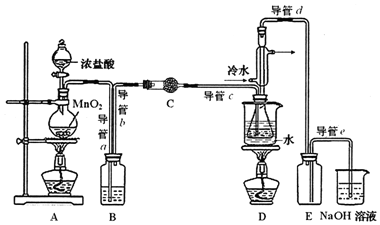
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
| S | 113 | 444 | 1.96 | 不溶于水 |
| S2Cl2 | -76 | 138 | 1.75 | 与水反应 |
| CS2 | -109 | 47 | 1.26 | 不溶于水 |
| CCl4 | -23 | 77 | 1.59 | 不溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com