
(12分)阿司匹林(乙酰水杨酸, )是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)
)是世界上应用最广泛的解热、镇痛和抗炎药。乙酰水杨酸受热易分解,分解温度为128~135℃。某学习小组在实验室以水杨酸(邻羟基苯甲酸)
 与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
与醋酸酐[(CH3CO)2O]为主要原料合成阿司匹林,制备基本操作流程如下:
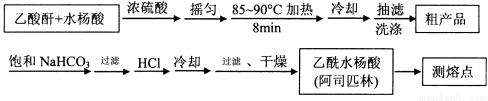
主要试剂和产品的物理常数

请根据以上信息回答下列问题:
(1)制备阿司匹林时,仪器应干燥,其原因是 。
该加热过程中,温度计控制 的温度
(2)写出制备阿司匹林的化学方程式 。
(3) ① 合成阿斯匹林时,加饱和NaHCO3的作用是 。
② 过滤所得粗产品要用少量冰水洗涤,则洗涤的具体操作是 。
(4)检验产品中是否含有水杨酸的试剂是 。
(5)该学习小组在实验中原料用量:2.0 g水杨酸、5.0 mL醋酸酐(ρ=1.08 g/cm3),最终称得产品m=2.1 g,则所得乙酰水杨酸的产率为 。
(1)防止乙酸酐水解(1分),85~90 ℃水浴(1分)
(2) (2分)
(2分)
(3)①使乙酰水杨酸生成易溶于水的乙酰水杨酸钠而达到分离的目的(2分),
②向漏斗中加冰水至浸没沉淀物,使洗涤剂缓慢通过沉淀物,重复上述操作2-3次(2分)
(4)FeCl3溶液(或溴水)(或其他合理的);(5)80. 5%(2分)。
【解析】
试题分析:(1)制备阿司匹林时,仪器应干燥,其原因是防止乙酸酐与水发生反应;该加热过程中,为了便于控制温度在水浴85~90 ℃,要水浴加热;(2)制备阿司匹林的化学方程式是: ;(3) ① 合成阿斯匹林时,加饱和NaHCO3的作用是使乙酰水杨酸生成易溶于水的乙酰水杨酸钠而达到分离的目的;② 过滤所得粗产品要用少量冰水洗涤可以减少物质的溶解损失。则洗涤的具体操作是向漏斗中加冰水至浸没沉淀物,使洗涤剂缓慢通过沉淀物,重复上述操作2-3次;(4)由于水杨酸含有酚羟基而阿司匹林无酚羟基,所以检验产品中是否含有水杨酸的试剂是用FeCl3溶液,若溶液变为紫色,则含有水杨酸;否则不含有;或用浓溴水,若产生白色沉淀,就含有水杨酸,否则不含有;(5)n(水杨酸)=2.0 g÷138g/mol=0.01449mol;n(醋酸酐)=(5.0 mL×ρ=1.08 g/cm3)÷102g/mol=0.053mol,根据方程式可知水杨酸不足量,应该按水杨酸来计算,理论产量是0.01449mol×180g/mol=2.60870g,实际最终称得产品m=2.1 g,则所得乙酰水杨酸的产率为(2.1 g÷2.6.87g)×100%=80. 5%
;(3) ① 合成阿斯匹林时,加饱和NaHCO3的作用是使乙酰水杨酸生成易溶于水的乙酰水杨酸钠而达到分离的目的;② 过滤所得粗产品要用少量冰水洗涤可以减少物质的溶解损失。则洗涤的具体操作是向漏斗中加冰水至浸没沉淀物,使洗涤剂缓慢通过沉淀物,重复上述操作2-3次;(4)由于水杨酸含有酚羟基而阿司匹林无酚羟基,所以检验产品中是否含有水杨酸的试剂是用FeCl3溶液,若溶液变为紫色,则含有水杨酸;否则不含有;或用浓溴水,若产生白色沉淀,就含有水杨酸,否则不含有;(5)n(水杨酸)=2.0 g÷138g/mol=0.01449mol;n(醋酸酐)=(5.0 mL×ρ=1.08 g/cm3)÷102g/mol=0.053mol,根据方程式可知水杨酸不足量,应该按水杨酸来计算,理论产量是0.01449mol×180g/mol=2.60870g,实际最终称得产品m=2.1 g,则所得乙酰水杨酸的产率为(2.1 g÷2.6.87g)×100%=80. 5%
考点:考查物质的制取原理、操作、方程式的书写、物质产率的计算的知识。


科目:高中化学 来源:2015届河北省衡水市高三上学期第一次月考化学试卷(解析版) 题型:填空题
(本题共10分)
(1)黄铁矿(FeS2)是生产硫酸和冶炼钢铁的重要原料.其中一个反应为3FeS2+8O2=6SO2+Fe3O4,氧化产物为 ,若有3mol FeS2参加反应,转移 mol电子。
(2)与明矾相似,硫酸铁也可用作净水剂,其原理为 (用离子方程表示)。
(3)FeCl3与氢碘酸反应时可生成棕色物质,该反应的离子方程式为 。
(4)在热的稀硫酸溶液中溶解一定量的FeSO4后,再加入足量的KNO3溶液,可使其中的Fe2+全部转化成Fe3+,并有气体逸出,请写出相应的离子方程式: 。
(5)铁红是一种红色颜料,其成分是Fe2O3将一定量的铁红溶于160mL 5mol?L-1盐酸中,在加入一定量铁粉恰好溶解,收集到2.24L(标准状况),经检测,溶夜中无Fe3+,则参加反应的铁粉的质量为 。
查看答案和解析>>
科目:高中化学 来源:2015届河北省石家庄市五校联考高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.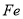 与稀
与稀 、稀
、稀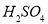 反应均有气泡产生,说明
反应均有气泡产生,说明 与两种酸均发生置换
与两种酸均发生置换
B. 中阴阳离子数数目之比为1:1
中阴阳离子数数目之比为1:1
C.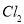 与
与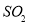 均能使品红褪色,说明二者均有氧化性
均能使品红褪色,说明二者均有氧化性
D.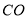 能够与人体里的血红蛋白结合,造成人体缺氧中毒
能够与人体里的血红蛋白结合,造成人体缺氧中毒
查看答案和解析>>
科目:高中化学 来源:2015届河北省唐山市高三10月月考理综化学试卷(解析版) 题型:填空题
【化学—选修3:物质结构与性质】(15分)
CuSO4在活化闪锌矿(主要成分是ZnS)方面有重要作用,主要是活化过程中生成CuS、Cu2S等一系列铜的硫化物活化组分。
(1)Cu2+基态的电子排布式可表示为 ;
(2)SO42-的空间构型为 (用文字描述);中心原子采用的轨道杂化方式是 ;写出一种与SO42-互为等电子体的分子的化学式: ;
(3) 向CuSO4 溶液中加入过量NaOH溶液可生成[Cu (OH)4 ]2-。不考虑空间构型,[Cu(OH)4]2-的结构可用示意图表示为 ;
(4)资料显示ZnS为难溶物,在活化过程中,CuSO4能转化为CuS的原因是 。
(5)CuS比CuO的熔点 (填高或低),原因是 。
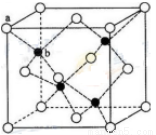
(6)闪锌矿的主要成分ZnS,晶体结构如下图所示,其晶胞边长为540.0 pm,密度为____________(列式并计算),a位置S2-离子与b位置Zn2+离子之间的距离为___________________pm(列式表示)。
查看答案和解析>>
科目:高中化学 来源:2015届河北省唐山市高三10月月考理综化学试卷(解析版) 题型:选择题
稀土是工业味精,邓小平同志说过“中东有石油,我们有稀土”。稀土元素铈(Ce)主要存在于独居石中,金属铈在空气中易氧化变暗,受热时燃烧,遇水很快反应。已知:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+。下列说法正确的是 ( )
A.电解熔融CeO2制Ce,铈在阳极获得
B.铈有四种稳定的核素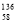 Ce、
Ce、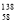 Ce、
Ce、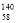 Ce、
Ce、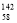 Ce,它们互为同素异形体
Ce,它们互为同素异形体
C.用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++Fe2+=Ce3++Fe3+
D.由于氧化性:Ce4+>Fe3+,而I—有强还原性,所以铈溶于氢碘酸的化学方程式可表示为:2Ce+6HI=2CeI3+3H2↑。
查看答案和解析>>
科目:高中化学 来源:2015届江西省红色六校高三第一次联考化学试卷(解析版) 题型:选择题
某合作学习小组讨论辨析以下说法:
①粗盐和酸雨都是混合物; ②纯碱和熟石灰都是碱;
③冰和干冰既是纯净物又是化合物; ④不锈钢和目前流通的硬币都是合金;
⑤盐酸和食醋既是化合物又是酸; ⑥N2O4是酸性氧化物,但不是酸酐;
⑦豆浆和雾都是胶体; ⑧  、
、 、
、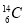 同种核素。
同种核素。
上述说法不正确的是( )
A.①②③④ B.①②⑤⑥ C.①③④⑦ D.②⑤⑥⑧
查看答案和解析>>
科目:高中化学 来源:2015届江西省红色六校高三第一次联考化学试卷(解析版) 题型:选择题
下列各组离子能大量共存,向溶液中通入足量相应气体后,各离子还能大量存在的是
A.氯气:K+ Ba2+ SiO32- NO3- B.二氧化硫:Na+ NH4+ SO32- C1-
C.氨气:K+ Na+ AlO2-. CO32- D.甲醛:Ca2+ Mg2+ MnO4- NO3-
查看答案和解析>>
科目:高中化学 来源:2015届江西省上学期高三第一次月考化学试卷(解析版) 题型:选择题
向含1mol HCl和1mol MgSO4的混合溶液中加入1mol/L的Ba(OH) 2溶液,产生沉淀的物质的量(n)与加入Ba(OH) 2溶液体积(V)间的关系图正确的是 ( )
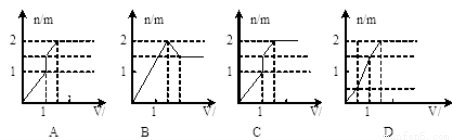
查看答案和解析>>
科目:高中化学 来源:2015届江西省新余市高三第二次模拟考试化学试卷(解析版) 题型:选择题
将一定量的钠铝合金置于水中,合金全部溶解,得到20 mL pH=14的溶液,然后用1mol/L的盐酸滴定,沉淀质量与消耗盐酸的体积关系如图所示,则下列选项正确的是
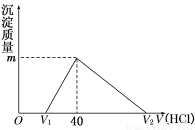
A.原合金质量为0.92 g B.标准状况下产生氢气896 mL
C.图中V2为60 mL D.图中m值为1.56 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com