
【题目】如图是工业制取菱镁矿MgCO3(含杂质Al2O3、FeCO3)制取镁的工艺流程

请回答有关问题:
(1)菱镁矿进入酸浸池前需要粉碎,目的是 __________________________。
(2)氧化池通入Cl2的目的是氧化 _________________________(填化学式),工业上不选用硝酸做氧化剂的原因是_________________和_________________________。
(3)物质甲可以是_____________
A、MgO B、Mg(OH)2 C、NaOH溶液 D、稀氨水
(4)由MgCl2溶液制取无水MgCl2的操作方法 __________________________。
(5)当Fe3+完全沉淀时,求最小pH__________。已知:氢氧化铁ksp=1.0×10-38,离子浓度小于1×10-5 mol/L认为沉淀完全
【答案】 增大接触面积,加快溶解速率 FeCl2 引入杂质离子NO3- 产生污染性气体氮氧化物 AB 在干燥的HCl气流中加热蒸干 3
【解析】(1)酸浸前将菱镁矿粉碎,可以增大接触面积,加快溶解速率;
(2)为除去溶液中的Fe2+,氧化池通入Cl2的目的是氧化FeCl2,如果用硝酸替换氯气做氧化剂,则会引入杂质离子NO3-,同时产生污染性气体氮氧化物;
(3)物质甲是调节溶液pH,使溶液中Fe3+沉淀完全,根据除杂不引入新杂质的原则,可以选择MgO或Mg(OH)2 ,故答案为AB;
(4)因加热能促进Mg2+,由MgCl2溶液蒸发结晶制取无水MgCl2时需要在干燥的HCl气流中加热蒸干;
(5)ksp=c(Fe3+)×c3(OH-)=1.0×10-38,当Fe3+离子浓度小于1×10-5 mol/L认为沉淀完全,此时c(OH-)=1.0×10-11mol/L,pH=3。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】利用如图所示装置测定中和热的实验步骤如下:
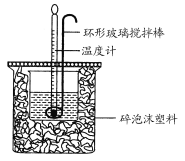
①用量筒量取50 mL 0.50 mol·L-1盐酸倒入小烧杯中,测出盐酸温度;
②用另一量筒量取50 mL 0.55 mol·L-1 NaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测得混合液最高温度,回答下列问题:
(1)为什么所用NaOH溶液要稍过量?_________________________
(2)倒入NaOH溶液的正确操作是______________(填序号)。
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(3)使盐酸与NaOH溶液混合均匀的正确操作是______________(填序号)。
A.用温度计小心搅拌 B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯 D.用套在温度计上的环形玻璃搅拌棒轻轻地搅动
(4)现将一定量的稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别和1 L 1 mol·L-1的稀盐酸恰好完全反应,其反应热分别为ΔH1、ΔH2、ΔH3,则ΔH1、ΔH2、ΔH3的大小关系为______________。
(5)______________(填“能”或“不能”)用Ba(OH)2溶液和硫酸代替氢氧化钠溶液和盐酸,理由是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一整套电化学装置如右图,关于该装置说法正确的是( )
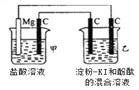
A. 甲池中Mg极为正极,电极反应式为:Mg-2e-═Mg2+
B. 甲池中C电极发生氧化反应
C. 乙池中将化学能转化为电能
D. 乙池左侧石墨电极附近变蓝,右侧石墨电极附近变红
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将V1 mL 1.0 mol·L-1 HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后,测量并记录溶液的温度,实验结果如下图所示,实验中始终保持V1+V2=50。

(1)对于反应:HCl+NaOH= NaCl+H2O,反应物所具有的总能量E1和生成物所具有的总能量E2的关系为:E1____E2。(填“>”、“ <”或“=”)
(2)实验中所用NaOH溶液的浓度为____mol·L-1。
(3)若含有8.0 g NaOH的稀溶液与稍过量的1 L 0.21 mol·L-1的盐酸反应放出11.46 kJ的热量,则表示中和热的热化学方程式为___________________。
(4)若取50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液置于如图所示的装置中进行中和热的测定实验,回答下列问题:
①从实验装置看,其中尚缺少的一种玻璃用品是_________;
实验序号 | 起始温度t1/℃ | 终止温度 (t2)℃ | ||
盐酸 | NaOH溶液 | 平均值 | ||
1 | 25.1 | 24.9 | 25.0 | 28.0 |
2 | 25.1 | 25.1 | 25.1 | 28.2 |
3 | 25.1 | 25.1 | 25.1 | 28.3 |
4 | 25.1 | 25.1 | 25.1 | 27.4 |
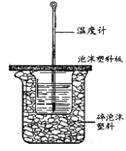
已知盐酸、NaOH溶液密度近似为1.00g/cm3,中和后混合液的比热容c=4.18kJ/(kg·K),根据上表数据,求出该反应的中和热△H=____________ (保留2位小数) ;
③上述实验数值结果与57.3 kJ/mol有偏差,产生偏差的原因可能是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Q、R、T、M、W五种短周期元素在周期表中的相对位置如图所示,其中M的原子序数是R的原子序数的2倍.下列说法正确的是( ) ![]()
A.MW6中各原子核外均满足8电子稳定结构
B.Q、W的单核离子的核外电子数相等
C.五种元素均能形成氢化物
D.W的氢化物水溶液酸性最强,说明W的非金属性在五种元素中最强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应2X(g)2Y(g)+2Z(g)△H>0达到平衡时,要使正反应速率降低,X的浓度增大,应采取的措施是( )
A.加压B.减压C.减小Z的浓度D.降温
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,把2. 0体积的N2和6. 0体积的H2通入一个带活塞的体积可变的容器中,活塞的一端与大气相通,容器中发生如下反应:N2+3H2![]() 2NH3。已知平衡时NH3的浓度是c mol·L-1,现按下列四种配比作为起始物质,分别充入上述容器,并保持温度不变,则达到平衡后,NH3的浓度不为c mol·L-1的是( )
2NH3。已知平衡时NH3的浓度是c mol·L-1,现按下列四种配比作为起始物质,分别充入上述容器,并保持温度不变,则达到平衡后,NH3的浓度不为c mol·L-1的是( )
A. 1.0体积的N2和3.0体积的H2
B. 2.0体积的N2和6.0体积的H2和4.0体积的NH3
C. 4.0体积的NH3和1.0体积的H2
D. 2.0体积的NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在容积为2L的密闭容器中发生反应CO(g)+H2O(g) ![]() CO2(g)+H2(g),部分数据见下表(表中t2>t1)
CO2(g)+H2(g),部分数据见下表(表中t2>t1)
反应时间/min | n(CO)/mol | n(H2O)/mol | n(CO2)/mol | n(H2)/mol |
0 | 1.20 | 0.60 | 0 | 0 |
t1 | 0.80 | |||
t2 | 0.20 |
下列说法正确的是
A. 反应在t1min末的速率为v(H2)=0.40/t1 mol·L-1·min-1
B. 平衡时CO的转化率为66.67%
C. 该温度下反应的平衡常数为1
D. 其他条件不变,若起始时,n(CO)=0.60 mol,n(H2O)=1.20 mol,则平衡时n(CO2)=0.20mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是
A. 硅主要以单质、氧化物、硅酸盐的形式存在于自然界中
B. 适量CO2通入漂白粉的水溶液可以生成白色沉淀
C. 在燃煤中加入石灰石可减少SO2的排放,发生的总反应为2CaCO3+2SO2+O2![]() 2CO2+2CaSO4
2CO2+2CaSO4
D. 不能用玻璃瓶来盛装氟化钠水溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com