
| A. | 向煤中加入适量CaSO4,可大大减少烟气中的SO2 | |
| B. | 为保证加酶洗衣粉的洗涤效果,应用温水溶解洗衣粉 | |
| C. | 明矾水解形成的胶体能吸附水中悬浮物,可用于水的净化 | |
| D. | 光导纤维在信息领域应用越来越广泛,光纤的主要成分是SiO2 |
分析 A.向煤中进入适量CaO除去煤中二氧化硫,而不是加入硫酸钙;
B.酶的主要成分为蛋白质,温水中可以提高酶的催化效果,增强洗涤效果;
C.明矾电离出的铝离子水解生成氢氧化铝胶体,氢氧化铝胶体具有较大吸附面积,可以净化水;
D.光导纤维的主要成分为二氧化硅,光导纤维广泛应用于信息领域.
解答 解:A.为减少燃烧产物中SO2的量,一般是向煤中加入适量生石灰CaO,故A错误;
B.酶在适宜的温度下,催化效果更好,所以为保证加酶洗衣粉的洗涤效果,应用温水溶解洗衣粉,故B正确;
C.明矾电离出的铝离子部分水解生成氢氧化铝胶体,氢氧化铝胶体能吸附水中悬浮物,可用于水的净化,故C正确;
D.光导纤维是一种新型无机材料,广泛应用于通信、信息处理等领域,其主要成分是SiO2,故D正确;
故选A.
点评 本题考查了二氧化硫的治理、酶的性质、二氧化硅的性质、水的净化等知识,难度难度知识,试题综合性较强、知识点较多,充分考查了学生的分析、理解能力及灵活应用基础知识的能力,试题将化学性质与实际生活向联系,增强了学生学习化学的兴趣.


科目:高中化学 来源: 题型:选择题
| A. | 中子数为20的氯原子:1720Cl | |
| B. | CO2的比例模型: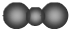 | |
| C. | 14C的原子结构示意图为 | |
| D. | CrO5的结构式为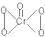 ,该氧化物中Cr为+6价 ,该氧化物中Cr为+6价 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
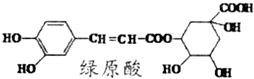
| A. | 分子中所有的碳原子均可能在同一平面内 | |
| B. | 1 mol绿原酸与足量溴水反应,最多消耗2.5mol Br2 | |
| C. | 绿原酸可以与FeCl3溶液发生显色反应 | |
| D. | 绿原酸不能发生消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
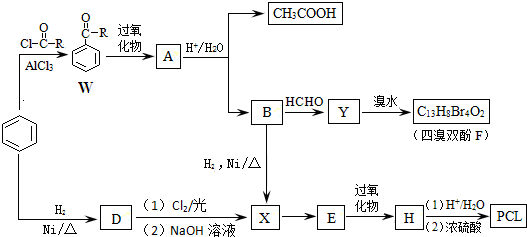
 .
.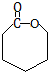 .
. .
. .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 阳离子 | NH4+、Na+、Mg2+ |
| 阴离子 | OH-、NO3-、SO42- |
| A. | 可能是Na2S04 | B. | 可能是NH4NO3 | C. | 可能是NaOH | D. | 一定不是(NH4)2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 +Br2$\stackrel{FeBr_{3}}{→}$
+Br2$\stackrel{FeBr_{3}}{→}$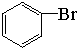 +HBr.
+HBr.| A. | ③④ | B. | ①② | C. | ②③ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
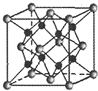 (1)X、Y、Z三种短周期元素,其中X的一种核素是最简单的原子,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子.
(1)X、Y、Z三种短周期元素,其中X的一种核素是最简单的原子,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com