
【题目】某有机物是一种医药中间体。其结构简式如图所示,下列有关该物质的说法正确的是
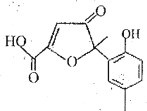
A.该化合物分子中只含一个手性碳原子
B.该化合物与NaHCO3溶液作用有CO2气体放出
C.1mol该化合物与足量溴水反应,消耗3molBr2
D.在一定条件下,该化合物与HCHO能发生缩聚反应
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:
【题目】下图是第3周期11~17号元素某些性质变化趋势的柱形图,下列有关说法中正确的是( )

A. y轴表示的可能是第一电离能
B. y轴表示的可能是电负性
C. y轴表示的可能是原子半径
D. y轴表示的可能是原子形成简单离子转移的电子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学为探究MnO2与浓盐酸的反应,用如图所示的装置进行实验。
(1)B是用来收集气体的装置,但未将导管画全,请在装置图中将导管补画完整。_________
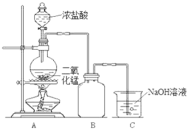
(2)制备实验开始时,先检查装置气密性,接下来的操作依次是_________(填字母)。
A.往烧瓶中加入MnO2粉末 B.加热 C.往烧瓶中滴加浓盐酸
(3)实验中该同学取8.7g MnO2和50mL 12mol/L浓盐酸在圆底烧瓶中共热,直到反应停止,最后发现烧瓶中还有固体剩余,该同学还检测到有一定量的盐酸剩余。
①MnO2与浓盐酸反应的化学方程式为_________。
②为什么有一定量的盐酸剩余但未能使MnO2完全溶解?_________。
③下列试剂中,能证明反应停止后烧瓶中有盐酸剩余的是_________(填字母)。
A.硝酸银溶液 B.碳酸钠溶液 C.氯化钠溶液
(4)为了测定反应残余液中盐酸的浓度,该同学设计了两个实验方案:
方案一:将A中产生的气体缓缓通过已称量的装有足量NaOH溶液的洗气瓶,反应停止后再次称量,两次质量差即是Cl2的质量,据此可求剩余盐酸的量。
方案二:当MnO2与浓盐酸的反应结束后,在装置A中加入足量的锌粉,用排水法测得产生H2的体积为V L(已换算为标准状况下)。
①实际上方案一不合理,原因为_________。
②根据方案二,写出剩余盐酸的物质的量浓度的计算式(假设反应前后溶液的体积保持不变)_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物完全燃烧生成CO2和水。将12g该有机物完全燃烧的产物通过浓硫酸,浓硫酸增重14.4g;再通过碱石灰,碱石灰增重26.4g,该有机物的分子式为( )
A. C4H10OB. C2H6OC. C3H8OD. C2H4O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1-溴丙烷在不同条件下的反应及各物质转化关系如图所示:
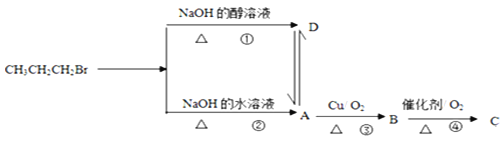
(1)D物质的结构简式为_____________,试写出反应②的化学反应方程式:________________。
(2)有机物A可以金属钠反应,试写出该反应的化学方程式_______________________________。
(3)B物质中可能含有的官能团是_________________。检验该官能团常用以下哪种试剂________
A. 浓硫酸 B.NaOH溶液 C.无水硫酸铜 D.新制氢氧化铜悬浊液
该反应的原理是____________________________________________(用化学方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化钠(Na3N)是科学家制备的一种重要的化合物,它与水作用可产生NH3。请回答下列问题:
(1)Na3N的电子式是__,该化合物是由__键形成。
(2)Na3N与盐酸反应生成__种盐,反应的化学方程式是__。
(3)比较Na3N中两种微粒的半径:r(Na+)___r(N3-)(填“>”、“=”、“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中某些气体的制取、收集及尾气处理装置如图所示(省略夹持和净化装置)。仅用此装置和表中提供的物质完成相关实验,最合理的选项是

选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 浓氨水 | CaO | NH3 | H2O |
B | 浓硫酸 | Na2SO3 | SO2 | NaOH溶液 |
C | 稀硝酸 | Cu | NO2 | H2O |
D | 浓盐酸 | MnO2 | Cl2 | NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化合物的结构如图所示,W、X、Y均为短周期元素,W+离子为短周期金属阳离子中半径最大的元素,Y元素形成的单质是理想的气体燃料。下列说法不正确的是( )
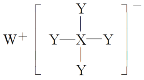
A.该化合物是强还原剂
B.Y-与Li+具有相同的电子层结构
C.X可能是碳元素或者是硅元素
D.原子半径大小关系为:W>X>Y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新能源汽车的核心部 件是锂离子电池,磷酸亚铁锂(LiFePO4)以其高倍率性、高比能量、高循环特征、高安全性、低成本、环保等优点而逐渐成为“能源新宠”。
[方法一]高温固相法是磷酸亚铁锂生产的主要方法。通常以亚铁盐(如FeC2O42H2O)磷酸盐和锂盐为原料,充分混匀后,在惰性气氛的保护气中先经过较低温预分解,再经过高温焙烧,研磨粉碎制成。其反应原理如下:
Li2CO3+2FeC2O42H2O+2NH4H2PO4 =2NH3↑+3CO2↑+ + +
(1)完成上述化学方程式______。
(2)理论上,反应中每转移0.15mol电子,会生成 ______gLiFePO4。
[方法二]以铁红、锂辉石LiAl(SiO3)2(含少量Ca2+、Mg2+的盐)、碳粉等原料来生产磷酸亚铁锂。其主要工艺流程如图:
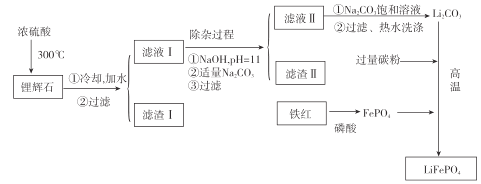
已知:2LiAl(SiO3)2+H2SO4(浓)![]() Li2SO4 + Al2O34SiO2H2O↓
Li2SO4 + Al2O34SiO2H2O↓
温度/℃ | 20 | 40 | 60 | 80 |
溶解度(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
溶解度(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.5 |
(1)向滤液II中加入饱和Na2CO3溶液,过滤后 ,用“热水洗涤”的原因是_____。
(2)滤渣II的主要成分是_______(填化学式)。
(3)写出在高温下生成磷酸亚铁锂的化学方程式:_____________。
(4)工业上,将 Li2CO3粗品制备成高纯 Li2CO3 的部分工艺如下:
①将粗产品Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择半透膜隔开,用惰性电极电解,阳极的电极反应式是____________。
②电解后向产品LiOH 溶液中加入过量 NH4 HCO3并加热,过滤、烘干得高纯 Li2CO3。 请写出生成Li2CO3的化学方程式:___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com