



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
 ̼��̼�Ļ������������������е�Ӧ�÷dz��㷺�����ᳫ���������ѳɳ����Ľ��죬����̼�������ֻ��һ�����룬����һ��ֵ���ڴ����µ����ʽ��
̼��̼�Ļ������������������е�Ӧ�÷dz��㷺�����ᳫ���������ѳɳ����Ľ��죬����̼�������ֻ��һ�����룬����һ��ֵ���ڴ����µ����ʽ��| ���� |
| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | |
| H2O | CO | CO2 | |||
| 1 | 650 | 2 | 4 | 1.6 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 3 |
| 3 | 900 | 1 | 2 | 0.4 | 1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ʵ���� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | �ﵽƽ������ʱ��/min | |
| H2O | CO | CO2 | |||
| 1 | 650 | 2 | 4 | 1.6 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 3 |
| 3 | 900 | 1 | 2 | 0.4 | 1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���㽭ʡ̨����ѧ2011��2012ѧ��߶���ѧ�����п��Ի�ѧ���� ���ͣ�058
��(N2H4)�ֳ���������һ�ֿ�ȼ��Һ�壬�������������ﷴӦ�������ɵ�����ˮ��������һ�������Դ��Һ����¾����������ȼ�ϣ�
����������ȡ�봢��������Դ����������о��ȵ㣮
��֪��CH4(g)��H2O(g)��CO(g)��3H2(g)����H����206.2 kJ��mol��1
CH4(g)��CO2(g)��2CO(g)��2H2(g)��H����247.4 kJ��mol��1
(1)������Ϊ����Դ���ŵ�________��(��2��)
(2)�Լ���Ϊԭ����ȡ�����ǹ�ҵ�ϳ��õ����ⷽ����CH4(g)��H2O(g)��Ӧ����CO2(g)��H2(g)���Ȼ�ѧ����ʽΪ________��
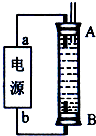
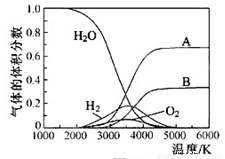
(3)H2O���ȷֽ�Ҳ�ɵõ�H2��������ˮ�ֽ���ϵ����Ҫ���������������¶ȵĹ�ϵ��ͼ��ʾ��ͼ��A��B��ʾ������������________��________��

��(4)��һ����ȼ�ϵ����һ�ּ���ȼ�ϵ�أ��������Һ��20����30����KOH��Һ���õ�طŵ�ʱ�������ĵ缫��Ӧʽ��________��
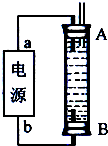
(5)��ͼ��һ���绯ѧװ��ʾ��ͼ������һ����ȼ�ϵ������װ�õĵ�Դ��

�����A�Dz��缫��B��ʯī�缫��C�����ᣭ����泥������ĵ缫��Ӧʽ��________��
�����ø�װ�ÿ��Ƶ������������⣺��������SO42����������S2O82��(�������������)��S2O82����H2O��Ӧ����H2O2��S2O82����2H2O��2SO42����H2O2��2H+����Ҫ��ȡ2 molH2O2����ȼ�ϵ��������������________molN2H4��
(6)��A��B��C��D���ֽ������±���װ�ý���ʵ�飮
ʵ��װ��������

����ʵ������ش��������⣺
��װ�ñ�����Һ��PH________��(������С�����䡱)
�����ֽ���������������ǿ��˳����________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013���㽭ʡ�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
��16�֣��£�N2H4���ֳ���������һ�ֿ�ȼ��Һ�壬�������������ﷴӦ�������ɵ�����ˮ��������һ�������Դ��Һ����¾����������ȼ�ϡ�
�� ��������ȡ�봢��������Դ����������о��ȵ㡣
��֪��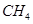 ��g��+
��g��+ 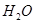 ��g��=
��g��=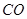 ��g��+
��g��+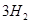 ��g��
��g�� 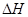 =
+
=
+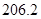

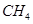 ��g��+
��g��+ 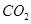 ��g��=
��g��=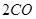 ��g��+
��g��+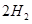 ��g��
��g��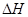 = +
= +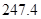

��1��������Ϊ����Դ���ŵ� ������2�㣩
��2���Լ���Ϊԭ����ȡ�����ǹ�ҵ�ϳ��õ����ⷽ����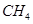 ��g����
��g����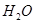 ��g����Ӧ����
��g����Ӧ����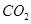 ��g����
��g����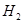 ��g�����Ȼ�ѧ����ʽΪ
��
��g�����Ȼ�ѧ����ʽΪ
��
��3��H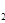 O���ȷֽ�Ҳ�ɵõ�H
O���ȷֽ�Ҳ�ɵõ�H ��������ˮ�ֽ���ϵ����Ҫ���������������¶ȵĹ�ϵ��ͼ��ʾ��ͼ��A��B��ʾ������������
�� ��
��������ˮ�ֽ���ϵ����Ҫ���������������¶ȵĹ�ϵ��ͼ��ʾ��ͼ��A��B��ʾ������������
�� ��
��4����һ����ȼ�ϵ����һ�ּ���ȼ�ϵ�أ��������Һ��20%��30%��KOH��Һ���õ�طŵ�ʱ�������ĵ缫��Ӧʽ�� ��
��5����ͼ��һ���绯ѧװ��ʾ��ͼ������һ����ȼ�ϵ������װ�õĵ�Դ��
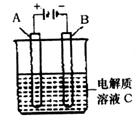
�����A�Dz��缫��B��ʯī�缫��C�����ᡪ����泥������ĵ缫��Ӧʽ�� ��
�����ø�װ�ÿ��Ƶ������������⣺��������SO42����������S2O82����������������ӣ���S2O82����H2O��Ӧ����H2O2��S2O82��+2H2O=2SO42��+H2O2+2H+����Ҫ��ȡ2molH2O2����ȼ�ϵ�������������� molN2H4��
��6����A��B��C��D���ֽ������±���װ�ý���ʵ�顣
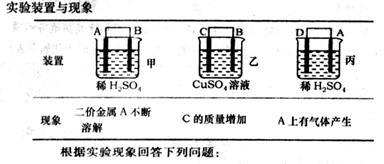
��װ�ñ�����Һ��P H ����������С�����䡱��
�����ֽ���������������ǿ��˳���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ���㽭ʡ������ ���ͣ������

 ��Ӧ����
��Ӧ���� ���Ȼ�ѧ����ʽΪ___________________ ��
���Ȼ�ѧ����ʽΪ___________________ ��


�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com