
分析 (1)根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶来分析需要的仪器;
(2)由于实验室无450mL容量瓶,故应选择500mL的容量瓶,故配制出500mL溶液.根据所需的氢氧化钾的质量m=CVM来计算;
(3)根据c=$\frac{n}{V}$并结合溶质的物质的量n和溶液的体积V的变化来进行误差分析;
(4)氢氧化钠的摩尔质量小于氢氧化钾.
解答 解:(1)由于实验室无450mL容量瓶,故应选择500mL的容量瓶,根据配制步骤是计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶可知所需的仪器为烧杯、玻璃棒、托盘天平、500mL容量瓶和胶头滴管,故答案为:500mL容量瓶;
(2)由于实验室无450mL容量瓶,故应选择500mL的容量瓶,故配制出500mL溶液.所需的氢氧化钾的质量m=CVM=0.1mol/L×0.5L×56g/mol=2.8g,
故答案为:2.8;
(3)定容时仰视,则溶液体积偏大,故浓度小于0.1mol/L,故答案为:<;
(4)由于氢氧化钠的摩尔质量小于氢氧化钾,故所称量的固体的物质的量偏大,则所配得溶液的c(OH-)浓度大于0.1mol/L,故答案为:>.
点评 本题考查了一定物质的量浓度溶液的配制,难度不大,注意计算的方法.


科目:高中化学 来源: 题型:选择题
| A. | 向某溶液中滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口,试纸不变蓝,则原溶液中无NH4+ | |
| B. | 向Ca(ClO)2溶液通入CO2,溶液变浑浊,再加入品红溶液,红色褪去 | |
| C. | 光照氯水有气泡冒出,该气体为Cl2 | |
| D. | 用四氯化碳萃取溴水中的溴后,分液时,有机层应从分液漏斗的上口倒出 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
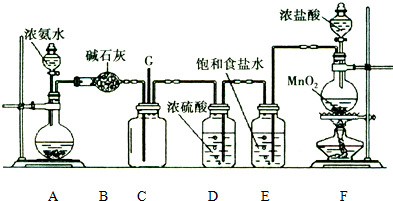
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,3.2gO2所含的原子数为0.2NA | |
| B. | 标准状况下,18gH2O所含的氧原子数目为NA | |
| C. | 常温常压下,92gNO2和N2O4的混合气体中含有的原子总数为6NA | |
| D. | 标准状况下,22.4L氦气与22.4L氟气所含原子数均为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝易氧化,但氧化铝具有保护内部铝的作用 | |
| B. | 铝的氧化物容易发生还原反应 | |
| C. | 铝不易被氧化 | |
| D. | 铝不易发生化学反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 测得0.1mol/L HA的pH>l | |
| B. | 测得NaA溶液的pH>7 | |
| C. | pH=l的HA溶液与盐酸稀释100倍后,盐酸的pH变化大 | |
| D. | 足量锌与相同pH、相同体积的盐酸和HA溶液反应,产生的氢气一样多 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 离子 | Fe3+ | Al3+ | Fe2+ | Mn2+ |
| 开始沉淀的pH | 2.7 | 3.7 | 7.0 | 7.8 |
| 沉淀完全的pH | 3.7 | 4.7 | 9.6 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 .
. .
. (或
(或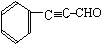 ).
). 、
、 、
、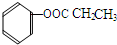 、
、 、
、 、
、 (写结构简式).
(写结构简式).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com