
| A. | 反应中硫酸做还原剂,有铜被还原 | |
| B. | NH4CuSO3中硫元素被氧化 | |
| C. | 2mol NH4CuSO3完全反应转移6.02×1023个电子 | |
| D. | 刺激性气味的气体是氨气 |
分析 NH4CuSO3与硫酸混合微热,生成红色固体物、产生有刺激性气味的气体和蓝色溶液,说明反应生成Cu、SO2和Cu2+,则NH4CuSO3中Cu的化合价为+1价,以此解答该题.
解答 解:反应的发产生为:2NH4CuSO3+4H+═Cu+Cu2++2SO2↑+2H2O+2NH4+.
A.由发产生为:2NH4CuSO3+4H+═Cu+Cu2++2SO2↑+2H2O+2NH4+,反应只有Cu元素的化合价发生变化,硫酸根反应前后未变,反应中硫酸体现酸性,故A错误;
B.NH4CuSO3与硫酸混合微热,生成红色固体物、产生有刺激性气味的气体和蓝色溶液,说明反应生成Cu、SO2和Cu2+,反应前后S元素的化合价没有发生变化,故B错误;
C.反应只有Cu元素的化合价发生变化,分别由+1→+2,+1→0,反应的发产生为:2NH4CuSO3+4H+═Cu+Cu2++2SO2↑+2H2O+2NH4+,每2molNH4CuSO3参加反应则转移1mol电子,则2mol NH4CuSO3完全反应转移6.02×1023个电子,故C正确;
D.因反应是在酸性条件下进行,不可能生成氨气,故D错误.
故选C.
点评 本题考查氧化还原反应,为高频考点,侧重考查学生的分析能力和计算能力,注意从反应现象判断生成物,结合化合价的变化计算电子转移的数目,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 杂化轨道的数目、形状和参与杂化的原子轨道数目、形状均相同 | |
| B. | 等性杂化轨道的形状、能量相等; NH3中N是等性杂化 | |
| C. | 各杂化轨道在空间应满足电子对互斥理论,以使排斥力最小 | |
| D. | sp3杂化轨道应由同原子里能量相同的s和p轨道杂化而得 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COOK(固体) | B. | CH3COOH | C. | KCl(固体) | D. | KOH(固体) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
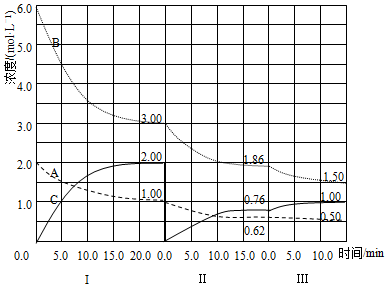
 工业上有一种用C02来生产甲醇燃料的方法:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1,将6mol CO2和8mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化如图所示(实线).图中数据a(1,6)表示:在1min时H2的物质的量是6mol.
工业上有一种用C02来生产甲醇燃料的方法:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1,将6mol CO2和8mol H2充入2L的密闭容器中,测得H2的物质的量随时间变化如图所示(实线).图中数据a(1,6)表示:在1min时H2的物质的量是6mol.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2.0gH218O与D2O的混合物中所含中子数为NA | |
| B. | 常温常压下,4.4g乙醛所含σ键数目为0.7 NA | |
| C. | 标准状况下,5.6L CO2与足量Na2O2反应转移的电子数为0.5 NA | |
| D. | 50ml 12mol/L盐酸与足量MnO2共热,转移的电子数为0.3 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
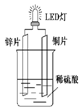 以Zn和Cu为电极,稀硫酸为电解质溶液形成的原电池,供LED发光,装置如图所示.
以Zn和Cu为电极,稀硫酸为电解质溶液形成的原电池,供LED发光,装置如图所示.
| 序号 | 甲 | 乙 | 丙 |
| 装置 |  | 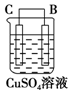 | 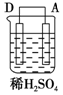 |
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 试剂 | 试纸或试液 | 现象 | 结论 |
| A | 浓氨水、生石灰 | 红色石蕊试纸 | 变蓝 | NH3为碱性气体 |
| B | 浓盐酸、浓硫酸 | pH试纸 | 变红 | HCl为酸性气体 |
| C | 浓盐酸、二氧化锰 | 淀粉-KI试液 | 先变蓝后褪色 | Cl2具有氧化性和漂白性 |
| D | 亚硫酸钠、硫酸 | 品红试液 | 褪色 | SO2具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
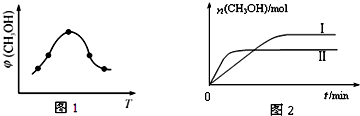 研究CO2的利用对促进低碳社会的构建具有重要意义.
研究CO2的利用对促进低碳社会的构建具有重要意义.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com