
取一小块金属钠,放在燃烧匙里加热,下列实验现象描述正确的是( )
①金属先熔化 ②在空气中燃烧,放出黄色火花 ③燃烧后得白色固体
④燃烧时火焰为黄色 ⑤燃烧后生成浅黄色固体物质
A.②⑤ B.①②③ C.①④⑤ D.④⑤
科目:高中化学 来源: 题型:
下列关于热化学反应的描述中正确的是( )
A.已知H+(aq)+OH-(aq) = H2O(l) ΔH=-57.3 kJ·mol-1,则H2SO4和Ba(OH)2反应的反应热
ΔH=2×(-57.3) kJ·mol-1
B.燃料电池中将甲醇蒸气转化为氢气的热化学方程式是:CH3OH(g)+ O2(g)=CO2(g)+2H2(g)
O2(g)=CO2(g)+2H2(g)
ΔH=-192.9 kJ·mol-1;则CH3OH(g)的燃烧热为192.9 kJ·mol-1
C.H2(g)的燃烧热是285.8 kJ·mol-1,则2H2O(g)=2H2(g)+O2(g)ΔH=+571.6 kJ·mol-1
D.葡萄糖的燃烧热是2800 kJ·mol-1,则  C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l)
C6H12O6(s)+3O2(g)=3CO2(g)+3H2O(l)
ΔH=-1400 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关金属元素特征的叙述中,正确的是( )
A.金属元素的原子只有还原性,离子只有氧化性
B.金属元素在化合物中一定显正价
C.金属元素在不同化合物中的化合价均不同
D.金属元素的单质常温下均为银白色固体
查看答案和解析>>
科目:高中化学 来源: 题型:
25 ℃、101 kPa下:①2Na(s) + 1/2O2(g)= Na2O(s) ΔH1= - 414 kJ·mol-1
② 2Na(s)+O2(g) = Na2O2(s) ΔH2= - 511 kJ·mol-1 , 下列说法正确的是 ( )
A.①和②产物的阴阳离子个数 比不相等
比不相等
B.①和②生成等物质的量的产物,转移电子数不同
C.25 ℃、101 kPa下,Na2O2(s)+2Na(s)=2Na2O(s) ΔH= - 317 kJ·mol-1
D.常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快
查看答案和解析>>
科目:高中化学 来源: 题型:
过氧化钠可作为氧气的来源。常温常压下二氧化碳和过氧化钠反应后,若固体质量增加了28 g,反应中有关物质的物理量正确的是(NA表示阿伏加德罗常数) ( )
| 二氧化碳 | 碳酸钠 | 转移的电子 | |
| ① | 1 mol | NA | |
| ② | 22.4 L | 1 mol | |
| ③ | 106 g | 1 mol | |
|
| 106 g | 2NA |
A.①③ B.②④ C.①④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
使5.6 L CO2气体迅速通过Na2O2固体后得到4.48 L(标准状况下)气体,这4.48 L气体的质量是 ( )
A.6.4 g B.8.2 g C.6.2 g D.8.8 g
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究性学习小组在做Na2O2与水反应实验时,发现向Na2O2与水反应后的溶液中滴加酚酞试液,溶液呈现 红色,但红色很快褪去,甲、乙、丙三位同学对此现象分别做了如下推测:
红色,但红色很快褪去,甲、乙、丙三位同学对此现象分别做了如下推测:
甲:因为反应后试管很热,所以可能是溶液温度较高使红色褪去。
乙:因为所加水的量较少,红色褪去可能是生成的NaOH溶液浓度较大。
丙 :Na2O2具有强氧化性,生成物中O2、H2O2(可能产物)等也具有强氧化性,可能是氧化漂白了红色物质。
:Na2O2具有强氧化性,生成物中O2、H2O2(可能产物)等也具有强氧化性,可能是氧化漂白了红色物质。
(1)验证甲同学的推测是否正确的方法是__________________________,验证乙同学的推测是否 正确的方法是_______________________________________
正确的方法是_______________________________________ ______;当出现__________
______;当出现__________ ________________现象时,即可说明丙同学的推测正确。
________________现象时,即可说明丙同学的推测正确。
(2)有同学提出用定量的方法探究丙同学的推测中是否含有H2O2,其实验方法为:称取2.6 g Na2O2固体,使之与足量的水反应,测量产生O2的体积,与理论值比较,即可得出结论 。
。
①测量气体体积时,必须待试管和量筒内的气体都冷却至室温时进行,应选用如图装置中的______________________________________________________,
理由是_________________________ _________________________________。
_________________________________。
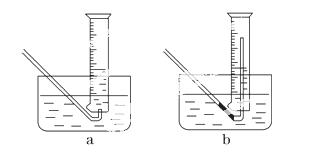
②若在标准状况下测量气体的体积,应选 用的量筒的大小规格为________(填“100 mL”、“200 mL”、“500 mL”或“1000 mL”)。
用的量筒的大小规格为________(填“100 mL”、“200 mL”、“500 mL”或“1000 mL”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
将等体积的HnRO3和Hn+1RO4两种酸溶液与定量的NaOH中和都生成正盐,则这两种酸的物质的量浓度比是( )
A.n∶(n+1) B.1∶1
C.1∶(n+1) D.( n+1)∶n
n+1)∶n
查看答案和解析>>
科目:高中化学 来源: 题型:
聚合氯化铝晶体是介于AlCl3和Al(OH)3之间的一种水溶性无机高分子聚合物,其制备原料主要是铝加工行业的废渣——铝灰,它主要含Al2O3、Al,还有SiO2等杂质。聚合氯化铝生产的工艺流程如下:
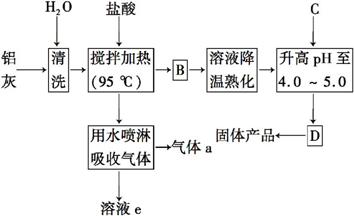
(1)反应中副产品a是 (用化学式表示)。
(2)升高pH至4.0~5.0的目的是______ 。
(3)生产过程中可循环使用的物质是 (用化学式表示)。
(4)为使得到的晶体较纯净,生产过程中使pH升高的C物质可选用 (填编号)。
a.NaOH b.Al c.氨水 d.Al2O3 e.NaAlO2
(5)聚合氯化铝晶体的化学式可表示为
[Al2(OH)nCl6-n·xH2O]m,实验室测定n的值:
①称取ag晶体,制成粉末,加热至质量不再变化为止,称量为bg。此过程可能用到的下列仪器有______ 。
a.蒸发皿 b.坩埚 c.研钵 d.试管
②另取ag晶体,进行如下操作:
用A试剂溶解→加足量AgNO3溶液→C操作→烘干→称量为cg。A试剂为_______(填试剂名称),C操作为 (填操作名称)。n= (用含b、c的代数式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com