


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:

| A、1mol维生素P最多可以和4mol溴水发生加成反应 |
| B、可溶于有机溶剂 |
| C、分子中有三个苯环 |
| D、1mol维生素P最多可以和5molNaOH反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 78 |
| 126 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 氯水滴入下列溶液中 | 实验现象 | 结论 |
| A | 滴有KSCN的FeCl2溶液 | 变红 | Cl2具有还原性 |
| B | 滴有酚酞的NaOH溶液 | 褪色 | Cl2具有漂白性 |
| C | 紫色石蕊溶液 | 先变红后褪色 | Cl2具有酸性、漂白性 |
| D | KI淀粉溶液 | 变蓝色 | Cl2具有氧化性 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、N2(g)+3H2(g)?2NH3 (g)△H=a kJ/mol |
| B、N2(g)+3H2(g)?2NH3 (g)△H=-a kJ/mol |
| C、N2(g)+3H2(g)?2NH3 (g)△H=5a kJ/mol |
| D、N2(g)+3H2(g)?2NH3(g)△H=-5a kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某溶液中加硝酸银溶液生成白色沉淀,说明原溶液中有Cl- |
| B、某溶液中加BaCl 2溶液生成白色沉淀,说明原溶液中有SO42- |
| C、某溶液中加NaOH溶液生成蓝色沉淀,说明原溶液中有Cu2+ |
| D、某溶液中加稀硫酸溶液生成白色沉淀,说明原溶液中有CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 浓硫酸 |
| 170℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
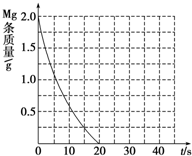 醋酸是一种常见的弱酸.
醋酸是一种常见的弱酸.| 实验 编号 | 温度 (K) | 盐酸浓度 (mol?L-1) | 醋酸浓度 (mol?L-1) | 实验目的 |
| a | 298 | 0.20 |  | Ⅰ.实验a和b是探究 Ⅱ.实验a和c是探究 Ⅲ.实验a和d是探究相同温度下,相同浓度的盐酸、醋酸与镁反应速率的区别 |
| b | 308 | 0.20 |  | |
| c | 298 | 0.40 |  | |
| d |  |  |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 向100mL NaOH溶液中,通入一定量CO2后,然后向该溶液中逐滴加入1mol?L-1硫酸,所加入硫酸溶液体积与产生CO2体积关系如图所示:
向100mL NaOH溶液中,通入一定量CO2后,然后向该溶液中逐滴加入1mol?L-1硫酸,所加入硫酸溶液体积与产生CO2体积关系如图所示:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com