D
分析:A、不同温度水的电离程度不同,水电离出的氢氧根离子和氢离子浓度相同,水的体积不知不能计算微粒数;
B、醋酸电离存在电离平衡.1mol分子电离生成2mol离子,溶液中含有水分子;
C、依据n=

计算物质的量,晶体硫酸氢钠是有钠离子和硫酸氢根离子构成;
D、乙烯和丙烯最简式相同为CH
2,计算56 gCH
2中碳原子数即可.
解答:A、pH=6的纯水中含有的 OH
-离子浓度 10
-6 mol/L,水的体积不知不能计算氢氧根离子数,故A错误;
B、醋酸电离存在电离平衡.1mol分子电离生成2mol离子,溶液中含有水分子;1 L 0.1 mol?L
-1的醋酸溶液中含有的离子和分子的总数大于 0.1 N
A,故B错误;
C、1.2 g NaHSO
4晶体物质的量为0.01mol,含有的阳离子和阴离子的总数为 0.02N
A,故C错误;
D、56 g乙烯和丙烯的混合气中含有的碳原子数,计算56 gCH
2中碳原子数=
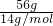
×N
A=4 N
A,故D正确;
故选D.
点评:本题考查阿伏伽德罗常数应用,主要考查弱电解质电离,物质构成离子判断,质量换算物质的量计算微粒数,题目难度中等.

 计算物质的量,晶体硫酸氢钠是有钠离子和硫酸氢根离子构成;
计算物质的量,晶体硫酸氢钠是有钠离子和硫酸氢根离子构成;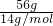 ×NA=4 NA,故D正确;
×NA=4 NA,故D正确;
