
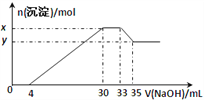
【题目】在100mL含Cu2+、Al3+、NH4+、H+、NO3-的溶液中,逐滴加入2.5mol·L-1NaOH溶液,所加NaOH 溶液的体积(mL)与产生沉淀的物质的量(mol)关系如下图所示。下列叙述正确的是( )
A. x-y=2×10-3mol
B. 原溶液中n(Cu2+)=0.025mol
C. 原溶液的pH=2
D. 原溶液中c(NH4+)=7.5×10-3mol·L-1
【答案】B
【解析】在100mL含Cu2+、Al3+、NH4+、H+、Cl-等离子的溶液中,逐滴加入2.5molL-1的NaOH溶液,加入4mLNaOH溶液时没有沉淀生成,说明H+先和NaOH反应,则溶液中含有H+,c(H+)=![]() =0.1mol/L,继续滴加NaOH溶液,沉淀的量逐渐增大,30mLNaOH溶液后,继续滴加NaOH溶液,沉淀的物质的量不变,则溶液中含有NH4+,则c(NH4+)=
=0.1mol/L,继续滴加NaOH溶液,沉淀的量逐渐增大,30mLNaOH溶液后,继续滴加NaOH溶液,沉淀的物质的量不变,则溶液中含有NH4+,则c(NH4+)=![]() =0.075mol/L,继续滴加NaOH,沉淀溶解,35mLNaOH后,沉淀不溶解,说明溶液中含有Cu2+、Al3+,根据Al3++3OH-=Al(OH)3↓、Al(OH)3+OH-=AlO2-+2H2O知,生成氢氧化铝沉淀和生成偏铝酸根离子需要氢氧化钠体积之比为3:1,则生成氢氧化铝沉淀需要NaOH体积=(35-33)mL×3=6mL,则生成氢氧化铜需要NaOH体积=(30-4mL)-6mL=20mL,则c(Cu2+)=
=0.075mol/L,继续滴加NaOH,沉淀溶解,35mLNaOH后,沉淀不溶解,说明溶液中含有Cu2+、Al3+,根据Al3++3OH-=Al(OH)3↓、Al(OH)3+OH-=AlO2-+2H2O知,生成氢氧化铝沉淀和生成偏铝酸根离子需要氢氧化钠体积之比为3:1,则生成氢氧化铝沉淀需要NaOH体积=(35-33)mL×3=6mL,则生成氢氧化铜需要NaOH体积=(30-4mL)-6mL=20mL,则c(Cu2+)=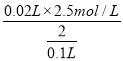 =0.25mol/L,c(Al3+)=
=0.25mol/L,c(Al3+)=![]() =0.05mol/L,溶液中存在电荷守恒,根据电荷守恒得3c(Al3+)+2c(Cu2+)+C(NH4+)+c(H+)=c(Cl-)=[3×0.05+2×0.25+0.075+0.1]mol/L=0.825mol/L;A.x为Al(OH)3、Cu(OH)2的物质的量,y为Cu(OH)2的物质的量,二者的差为Al(OH)3的物质的量=0.05mol/L×0.2L=0.01mol,故A错误;B.原溶液中n(Cu2+)=0.25mol/L×0.1L=0.025mol,故B正确;C.通过分析知,c(H+)=
=0.05mol/L,溶液中存在电荷守恒,根据电荷守恒得3c(Al3+)+2c(Cu2+)+C(NH4+)+c(H+)=c(Cl-)=[3×0.05+2×0.25+0.075+0.1]mol/L=0.825mol/L;A.x为Al(OH)3、Cu(OH)2的物质的量,y为Cu(OH)2的物质的量,二者的差为Al(OH)3的物质的量=0.05mol/L×0.2L=0.01mol,故A错误;B.原溶液中n(Cu2+)=0.25mol/L×0.1L=0.025mol,故B正确;C.通过分析知,c(H+)=![]() =0.1mol/L,所以pH=1,故C错误;D.通过以上分析知,c(NH4+)=
=0.1mol/L,所以pH=1,故C错误;D.通过以上分析知,c(NH4+)=![]() =0.075mol/L,故D错误;故答案为B。
=0.075mol/L,故D错误;故答案为B。


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
A. 含有离子键的化合物必是离子化合物
B. 含有共价键的化合物就是共价化合物
C. 共价化合物可能含离子键
D. 离子化合物中一定含有共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在由铜片、锌片和200mL稀硫酸组成的原电池中,若锌片口只发生电化学腐蚀,当在铜片上共放出2.24L气体(标准状况)时,稀H2SO4刚好用去一半,则产生这些气体消耗锌g,共有mol电子通过导线,原H2SO4溶液的浓度是mol/L.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com