
| A. | H2SO4?2H++SO42- | B. | BaCl2═Ba2++2Cl- | ||
| C. | NH3•H2O═NH4++OH- | D. | Na2CO3═Na++CO32- |
分析 强电解质完全电离用等号;弱电解质部分电离用可逆号;电离方程式遵循原子个数、电荷数守恒规律,据此解答.
解答 解:A.硫酸为强电解质,完全电离,电离方程式:H2SO4=2H++SO42-,故A错误;
B.氯化钡为强电解质,完全电离,电离方程式:BaCl2═Ba2++2Cl-,故B正确;
C.一水合铵为弱电解质,部分电离,电离方程式:NH3•H2O?NH4++OH-,故C错误;
D.碳酸钠为强电解质,完全电离,电离方程式:Na2CO3═2Na++CO32-,故D错误;
故选:B.
点评 本题考查了电解质电离方程式的书写,明确电解质强弱及电离方式是解题关键,注意电离方程式遵循原子个数、电荷数守恒规律,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 取样,滴加硫氰化钾溶液 | |
| B. | 取样,加足量的浓NaOH溶液加热,用湿润的红色石蕊试纸检验气体 | |
| C. | 取样,逐滴滴入氢氧化钠溶液直至足量 | |
| D. | 取样,加足量盐酸加热,湿润的品红试纸检验气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
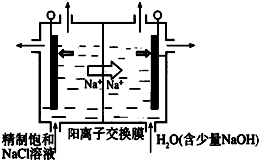 二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.目前已开发出用电解法制取ClO2的新工艺
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.目前已开发出用电解法制取ClO2的新工艺查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉、纤维素和油脂都是天然高分子化合物 | |
| B. | 石油的分馏、煤的干馏、石油的裂解都是化学变化 | |
| C. | 铝的还原性很强,铝热反应可以冶炼Fe、V、Cr等难熔化金属 | |
| D. | 工业上通过电解熔融的氯化物制取Na、Mg、Al三种金属 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
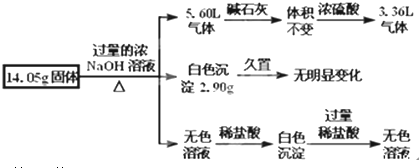
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
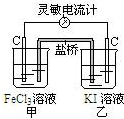
| A. | 反应开始时,乙中石墨电极上发生还原反应 | |
| B. | 反应开始时,甲中石墨电极上Fe3+被氧化 | |
| C. | 盐桥中的K+向乙中迁移,Cl-向甲中迁移 | |
| D. | 电流计读数为零后,在甲中溶入FeCl2固体,乙中石墨电极为正极 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④ | B. | ③④⑤ | C. | ④⑥⑦ | D. | ①②⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com