
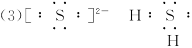
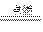 Na2O2 2Na2O2+2H2O====4NaOH+O2↑
Na2O2 2Na2O2+2H2O====4NaOH+O2↑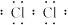 溶液变浑浊
溶液变浑浊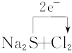 ="===2NaCl+S↓ " S2-+Cl2====S↓+2Cl-
="===2NaCl+S↓ " S2-+Cl2====S↓+2Cl-

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.离子化合物中可能含共价键,共价化合物中不含离子键 |
| B.共价化合物中可能含离子键,离子化合物中只含离子键 |
| C.构成单质分子的粒子一定含有共价键 |
| D.在氧化钠中,除氧离子和钠离子的静电吸引作用外,还存在电子与电子、原子核与原子核之间的排斥作用 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①④ | B.②④ |
| C.①②③ | D.①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com