
| A、两溶液的物质量浓度相同 |
| B、用同浓度的盐酸中和时,消耗盐酸的体积相同 |
| C、升高温度10℃,两溶液的pH仍相等 |
| D、两溶液中OH-离子浓度相同 |


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
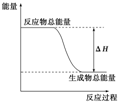 下列物质间的反应,其能量变化符合图的是( )
下列物质间的反应,其能量变化符合图的是( )| A、由氢气与氧气反应 |
| B、灼热的炭与二氧化碳反应 |
| C、Ba(OH)2?8H2O晶体和NH4Cl晶体混合 |
| D、碳酸钙的分解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、卤素单质与水反应均可用X2+H2O=HXO+HX表示 |
| B、HX都极易溶于水,它们的热稳定性随X的核电荷数的增加而减小 |
| C、卤素单质的颜色由F2→I2按相对分子质量增大而变深 |
| D、X-的还原性依次为:F-<Cl-<Br-<I- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、金属单质和盐溶液的反应都属于置换反应 |
| B、质量数相等的不同核素,一定属于不同种元素 |
| C、Al2O3既能与强碱反应,又能与强酸反应,所以Al2O3属于两性氧化物 |
| D、等物质的量的C2H6和H2O2含电子数相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
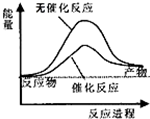
| A、如图可表示水分解过程中的能量变化 |
| B、高温高压下的超临界水,溶液中的氢离子和氢氧根离子浓度较大,有时显酸性,有时显碱性 |
| C、需要加热的反应一定是吸热反应,常温下能发生的反应一定是放热反应 |
| D、等体积、等浓度的醋酸钠溶液和次氯酸钠溶液中,所含离子总数,前者小于后者 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、随着核电荷数的增加,单质与水反应的剧烈程度增大 |
| B、随着核电荷数增加,单质的熔点.沸点升高 |
| C、随着核电荷数增加,它们的密度逐渐减小 |
| D、随着核电荷数增加,离子的氧化性逐渐增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加入溴水振荡,观察水层是否有棕红色出现 |
| B、滴入AgNO3溶液,再加入稀硝酸呈酸性,观察有无白色沉淀生成 |
| C、加入NaOH溶液共热,然后加入稀硝酸呈酸性,再滴入AgNO3溶液,观察有无白色沉淀生成 |
| D、加入NaOH溶液共热,冷却后滴入AgNO3溶液,观察有无白色沉淀生成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com