
| X |
| X |
| ||
| △ |
| ||
| △ |


科目:高中化学 来源: 题型:
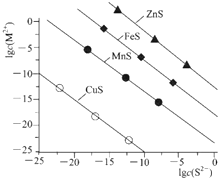 25℃时,用Na2S沉淀Cu2+、Mn2+、Fe2+、Zn2+四种金属离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)关系如图所示.下列说法正确的是( )
25℃时,用Na2S沉淀Cu2+、Mn2+、Fe2+、Zn2+四种金属离子(M2+),所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)关系如图所示.下列说法正确的是( )| A、Ksp(CuS)约为l×10-20 |
| B、向Cu2+浓度为10-5mol?L-1废水中加入ZnS粉末,会有CuS沉淀析出 |
| C、向l00mL浓度均为10-5mol?L-1 Zn2+、Fe2+、Mn2+的混合溶液中逐滴加入10-4mol?L-1 Na2S溶液,Zn2+先沉淀 |
| D、Na2S溶液中:2c(S2-)+2c(HS-)+2c(H2S)=c(Na+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 序号 | 实验器材 | 实验药品 | 实验目的 |
| A | 托盘天平(带砝码)、100mL容量瓶、量筒、烧杯、药匙、玻玻棒 | NaCl固体、蒸馏水 | 配制100 mL一定物质的量浓度的NaCl溶液 |
| B | 大试管、长颈漏斗、有孔塑料板、导管及橡皮塞、集气瓶、玻璃片、火柴 | 稀盐酸、块状石灰石 | 制取并收集二氧化碳气体 |
| C | 碱式滴定管、酸式滴定管、胶头滴管、铁架台(带铁夹)、锥形瓶 | 己知浓度的NaOH溶液、待测盐酸、蒸馏水、白纸 | 测定稀盐酸的物质的量浓度 |
| D | 铁架台(带铁夹)、酒精灯、大试管、集气瓶、导管及橡皮塞 | 氯化铵 | 制取并收集氨气 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝片放入NaOH溶液中:2Al+2OH-+6H2O=2[Al(OH)4]-+3H2↑ |
| B、NaHCO3电离:NaHCO3?Na++H++CO32- |
| C、醋酸与碳酸钠反应:2H++CO32-=CO2↑+H2O |
| D、铜与氯化铁溶液反应:Fe3++Cu=Cu2++Fe2+. |
查看答案和解析>>
科目:高中化学 来源: 题型:
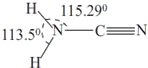
| A、既有酸性也有碱性 |
| B、既能溶于水,又能溶于乙醇 |
| C、分子内σ键与π键数目之比为1:1 |
| D、分子内中所有原子共面 |
查看答案和解析>>
科目:高中化学 来源: 题型:
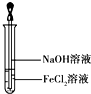 金属及其化合物在人类生活、生产中发挥着重要的作用.
金属及其化合物在人类生活、生产中发挥着重要的作用.查看答案和解析>>
科目:高中化学 来源: 题型:
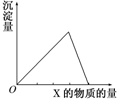 把X溶液(或气体)慢慢加入(或通入)到一定量的Y溶液中,产生的沉淀量与加入(或通入)的X物质的量的关系如图所示,符合图中曲线的是( )
把X溶液(或气体)慢慢加入(或通入)到一定量的Y溶液中,产生的沉淀量与加入(或通入)的X物质的量的关系如图所示,符合图中曲线的是( )| A、X为CO2,Y为Ca(OH)2 |
| B、X为NH3?H2O,Y为AlCl3 |
| C、X为NaOH,Y为AlCl3 |
| D、X为HCl,Y为NaAlO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na2O2溶于水产生O2:2O22-+2H2O═O2↑+4OH- |
| B、向氨水通入足量SO2:SO2+2NH3?H2O═2NH4++SO32-+H2O |
| C、次氯酸钠与浓盐酸反应产生Cl2:ClO-+Cl-+H2O═Cl2↑+2OH- |
| D、碳酸氢钠溶液和少量氢氧化钡溶液混合:Ba2++2OH-+2HCO3-═BaCO3↓+CO32-+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com