
(14分)某课外小组同学拟用乙醇分解法制乙烯,并对该反应进行探究。
(1)实验室制取乙烯的化学方程式为: ;
实验过程中,可观察到混合液变黑,产生有刺激性气味的气体。某研究小组同学经分析、讨论后认定:此现象是在该反应条件下,浓硫酸与乙醇发生氧化还原反应所致。
(2)为证明产物中混有SO2、CO2气体,甲同学设计了如下实验装置

他认为,只要观察到品红褪色,澄清石灰水变浑浊,就可确证混合气体中一定存在有SO2、CO2。你认为此看法是否正确 (填“是”或“否”),理由是 。
(3)为探究乙烯与Br2的反应,乙同学将制取的乙烯气体分别通过: NaOH溶液, Ba(OH) 2溶液,后用排水法收集于1000 mL的圆底烧瓶中(塞好橡皮塞),然后打开橡皮塞,向烧瓶中一次性加入1.5 mL液溴,塞上配有带乳胶管(用止水夹夹紧)的尖嘴玻璃管,摇荡,可观察到瓶内红棕色逐渐消失。然后按下图装好装置,打开止水夹,可观察到有喷泉形成,静置一段时间后,在溶液下部,有一层无色油状液体(约1.5 mL)。

①将乙烯气体通过Ba(OH) 2溶液的目的是 ;
②用化学方程式和简单的文字表述说明产生喷泉的原因_____________ ; ;
③请利用上述喷泉实验反应的产物设计一个简单实验,证明乙烯与Br2发生的是加成反应而不是取代反应 。
(1)CH3CH2OH CH2=CH2↑+H2O;
CH2=CH2↑+H2O;
(2)否;品红溶液褪色说明混合气体中存在SO2,但SO2气体也能使澄清石灰水变浑浊,其不一定被品红溶液完全吸收,故难以判断CO2 是否存在。
(3)① 确认其中的SO2、CO2均已被除尽(实验过程中溶液不会变浑浊)
② CH2=CH2 + Br2 → Br-CH2-CH2-Br,溴跟乙烯气体发生加成反应,生成液态的1,2-溴乙烷,导致烧瓶内压强减小,大气压将水压入烧瓶形成喷泉。
③ 取少量烧瓶中的水层液体,用pH 试纸测定,发现不呈酸性,说明无取代反应产物HBr生成。故发生的是加成反应。
【解析】
试题分析:(1)在实验室中是用浓硫酸与乙醇共热170℃制取乙烯的,化学方程式为CH3CH2OH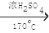 CH2=CH2↑+H2O;(2)由于SO2有漂白性,可以使品红溶液褪色,同时还可以与Ca(OH)2发生反应产生难溶液水的CaSO3白色沉淀。因此只观察到品红褪色,澄清石灰水变浑浊,只能确证混合气体中一定存在有SO2,但是不能确定是否含有CO2。(3)① 在制取的乙烯气体中含有SO2、CO2,通过前边的实验可能未被除去,因此通过Ba(OH) 2溶液的目的是确认其中的SO2、CO2均已被除尽;②溴跟乙烯气体发生加成反应,生成液态物质1,2-溴乙烷,导致烧瓶内气体压强减小,大气压将水压入烧瓶形成喷泉。用化学方程式表示是CH2=CH2 + Br2 → Br-CH2-CH2-Br,③ 检验喷泉实验反应的产物是乙烯与Br2发生的是加成反应而不是取代反应。根据反应产物继续判断,若是发生取代反应,则反应后溶液的酸性增强,若是发生加成反应,则反应后溶液酸性减弱。实验方法是取少量烧瓶中的水层液体,用pH 试纸测定,发现不呈酸性,说明无取代反应产物HBr生成。故发生的是加成反应。
CH2=CH2↑+H2O;(2)由于SO2有漂白性,可以使品红溶液褪色,同时还可以与Ca(OH)2发生反应产生难溶液水的CaSO3白色沉淀。因此只观察到品红褪色,澄清石灰水变浑浊,只能确证混合气体中一定存在有SO2,但是不能确定是否含有CO2。(3)① 在制取的乙烯气体中含有SO2、CO2,通过前边的实验可能未被除去,因此通过Ba(OH) 2溶液的目的是确认其中的SO2、CO2均已被除尽;②溴跟乙烯气体发生加成反应,生成液态物质1,2-溴乙烷,导致烧瓶内气体压强减小,大气压将水压入烧瓶形成喷泉。用化学方程式表示是CH2=CH2 + Br2 → Br-CH2-CH2-Br,③ 检验喷泉实验反应的产物是乙烯与Br2发生的是加成反应而不是取代反应。根据反应产物继续判断,若是发生取代反应,则反应后溶液的酸性增强,若是发生加成反应,则反应后溶液酸性减弱。实验方法是取少量烧瓶中的水层液体,用pH 试纸测定,发现不呈酸性,说明无取代反应产物HBr生成。故发生的是加成反应。
考点:考查实验室制取乙烯的反应原理、产物成分的确定、操作方法、乙烯的性质、喷泉实验原理及反应产物的检验方法的知识。


 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案科目:高中化学 来源:2014-2015福建省高二上学期期中化学(文)试卷(解析版) 题型:选择题
下列物质不属于“城市空气质量日报”报道的是
A.二氧化硫 B.氮氧化物 C.二氧化碳 D.悬浮颗粒
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省绥化市三校高一上学期期末联考化学试卷(解析版) 题型:选择题
下列物质不能通过化合反应直接制得的是
A.FeCl2 B.NaHCO3 C.Al(OH)3 D.Fe3O4
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三1月份阶段测试化学试卷(解析版) 题型:选择题
下列说法正确的是
A.按系统命名法,化合物 的名称是2,5,5—三甲基—3—乙基庚烷
的名称是2,5,5—三甲基—3—乙基庚烷
B.将 与NaOH的醇溶液共热可制备CH3—CH═CH2
与NaOH的醇溶液共热可制备CH3—CH═CH2
C.向柠檬醛 中加入酸性高锰酸钾,若溶液褪色,说明分子中含有醛基
中加入酸性高锰酸钾,若溶液褪色,说明分子中含有醛基
D. 、
、 、
、 三种氨基酸脱水,最多可生成6种二肽。
三种氨基酸脱水,最多可生成6种二肽。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三1月份阶段测试化学试卷(解析版) 题型:选择题
下列关于有机化合物的结构、性质的叙述正确的是
A.苯、油脂均能使酸性KMnO4溶液褪色
B.甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应
C.蔗糖、麦芽糖的分子式均为C12H22O11,二者互为同分异构体
D.乙醇、乙酸均能与NaOH稀溶液反应,因为分子中均含有官能团“—OH ”
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津南开区高三上学期第三次月考理综化学试卷(解析版) 题型:选择题
下列反应的离子方程式书写正确的是
A.往澄清石灰水中通入过量二氧化碳:Ca2++2OH-+CO2 = CaCO3↓+H2O
B.以石墨作电极电解氯化铝溶液:2Cl-+2H2O 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
C.硫酸亚铁溶液与稀硫酸、双氧水混合:2Fe2++H2O2+2H+ = 2Fe3++2H2O
D.少量硫酸氢钠溶液和氢氧化钡溶液混合:Ba2++SO42 -+2H++2OH-=BaSO4↓+2H2O
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省攀枝花市高三上学期第二次统考理综化学试卷(解析版) 题型:实验题
(14分)为了探究二氧化硫的漂白作用到底是二氧化硫本身还是二氧化硫与水作用的产物,某学习小组设计了如图装置来进行实验。

请回答下列问题:
(1)亚硫酸钠与浓硫酸反应的化学方程式是 。
为了探究干燥的SO2 能不能使品红褪色,请指出设计的实验装置图中两个明显的不足:① ;② 。
(2)按照修改后的装置,实验中控制SO2以大约每秒3个气泡的速度通过品红的酒精溶液时,经过一小时后,品红仍不褪色。这说明品红褪色的原因不是SO2直接导致。为此,SO2 通过品红水溶液后,引起品红褪色的微粒可能是 。
(3)甲同学实验如下:取等量、相同浓度的品红水溶液于两支试管中,再分别加入少量亚硫酸钠固体和亚硫酸氢钠固体,两支试管中的品红都褪色,对此,他得出结论:使品红褪色的微粒是HSO3-、SO32- ,不是H2SO3。乙同学认为他的结论不正确, 其理由是 。
(4)为了进一步探究,乙组同学做了如下实验:分别取相同浓度的品红溶液各20mL加入两只小烧杯中,两只烧杯中同时一次性各加入20mL0.1mol/L的亚硫酸钠溶液和20mL0.1mol/L的亚硫酸氢钠溶液,发现加入亚硫酸钠溶液的品红褪色明显较快。小组同学分别比较了两种溶液中各微粒浓度与褪色快慢的关系,得出的结论是 ,理由是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省达州市普高高三上学期第一次诊断理综化学试卷(解析版) 题型:选择题
下列有关说法不正确的是
A.SO42-的空间构型是正四面体形
B.CS2分子中各原子均达8电子稳定结构
C.CH3COOH分子中碳原子的杂化类型有sp2和sp3两种
D.H2O2分子是既含极性键又含非极性键的非极性分子
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市普陀区高三一模化学试卷(解析版) 题型:选择题
H2C2O4是一种二元弱酸,NaHC2O4溶液显酸性。现测得某溶液中存在的离子有C2O42-、HC2O4-、OH-、Na+、H+。下列判断正确的是
A.该溶液的溶质只能是Na2C2O4或NaHC2O4或两者的混合物
B.该溶液可能显酸性、碱性或中性
C.溶液中一定存在c(Na+) > c(HC2O4- )
D.溶液中一定存在c(H+) - c(OH-) > c(HC2O4- ) - c(Na+)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com