
����Ŀ���������������ơ���װ��ʹ�÷�������ѧ��ѧʵ��Ļ�������ͼΪ����ʵ��װ�á�

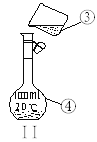
(1)д���������������ƣ�
��___________����__________����___________��
(2)������װ��I�������Ȼ�̼�;ƾ��Ļ�����ȱ�ٵ�������__________��������������������е�ʵ�����������Ϊ��_________���������е�ˮ����______��______��������ĸ���ţ���
(3)��������250 mL 0.2 mol��L NaCl��Һ��װ��II��ijͬѧת����Һ��ʾ��ͼ��ͼ�еĴ�����__________________________________��
���𰸡�ֱ�������� ��ƿ 1000mL������ƿ �ƾ��� ���� g f ��ʹ��250mL������ƿ�����ò���������
��������
(1)����װ���ص㣬��Ϊֱ�������ܣ�����ƿ����Ϊ1000mL������ƿ��
(2)������ķ�������е㲻ͬ��Һ�壬ʹ�þƾ��ƽ��м��ȣ�������ˮ������Ϊ�½��ϳ���
(3)����250 mL��Һ����Ҫ250mL������ƿ����Һʱ���ò�����������
(1)����װ���ص㣬��Ϊֱ�������ܣ�����ƿ����Ϊ1000mL������ƿ��
(2)������ķ����������Ȼ�̼�;ƾ��Ļ���ʹ�þƾ��ƽ��м��ȣ�������ˮ������Ϊ�½��ϳ�����g��f����
(3)����250 mL 0.2 mol/L NaCl��Һ����Ҫ250mL������ƿ����Һʱ���ò�����������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й����غϳ���(����)ʹ��������Ϊŷ�����ҵ�1/4��Ϊ�˱��������о�Ժ��ij������ʴ���̽����о����ó����и�ʴ������
(1)H2S���Ժϳ����ص���Ȼ������380K�����Ϊ2L���ܱ������У����ڷ�Ӧ��H2(g)��S(s)![]() H2S(g) ��H����21.6 kJ��mol��1����Ӧ�ﵽƽ��ʱ��H2��S��H2S�����ʵ�����Ϊ3 mol��
H2S(g) ��H����21.6 kJ��mol��1����Ӧ�ﵽƽ��ʱ��H2��S��H2S�����ʵ�����Ϊ3 mol��
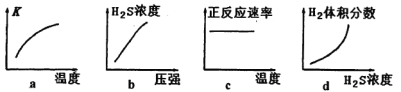
��380Kʱ�÷�Ӧ�Ļ�ѧƽ�ⳣ��Ϊ__________��
�����жԸ÷�Ӧ������ȷ����_________(�����)��
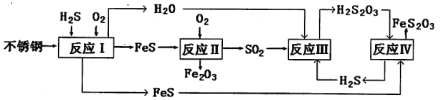
(2)��ӦII�Ļ�ѧ����ʽΪ��____________________________________��
(3)��֪������H2S2O3��K1��2.2��10��1��K2��2.5��10��2��
��Na2S2O3ˮ��Һ�е���غ�ʽΪ___________________________��
�ڷ�ӦIV�Ļ�ѧ����ʽ_____________________________________���÷�Ӧ_________(������������������)˵��FeS�ܽ���ǿ��FeS2O3��
(4)�����������ո�ʴ����Ϊ__________________��Ϊ����Ч���������ֽ������������������CuSO4��Һ������(H2S)�������ӷ�Ӧ����ʽΪ_________��(�����£�H2S��K1��1.3��10��7��K2��7.1��10��15��CuS��Ksp��6.3��10��36)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ClO2������һ�ָ�Ч�����ס���ȫ��ɱ��������������NaClO3�Ͳ��ᣨH2C2O4����Ӧ�Ƶá���ˮ����100�����������ijѧϰС������ͼװ��ģ�ҵ��ȡ�ռ�ClO2 ��
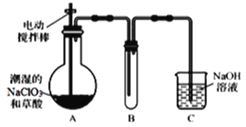
��1��ʵ��ʱװ��A����60��~100����е�ԭ����_________�����������¶ȵķ�����________��
��2��װ��A�з�Ӧ������Na2CO3��ClO2��CO2�ȣ��÷�Ӧ�Ļ�ѧ����ʽΪ___________��
��3����װ��C��ClO2��NaOH��Ӧ���ɵ����ʵ����������Σ�����һ����ΪNaClO2 ��д����Ӧ�����ӷ���ʽ_________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���й���ѧԺ�����Ŷ��о��������ڳ��³�ѹ�Ϳɼ����£�����LDH(һ�ֹ������)�ϳ�NH3��ԭ��ʾ��ͼ������˵������ȷ����

A.�ù�����H2O����ԭ��������
B.�ù������漰���Լ��ͷǼ��Լ��Ķ���������
C.���ںϳ�NH3�Ĺ������ڵ��Ĺ̶�
D.�ù��̵Ļ�ѧ����ʽΪ��2N2��6H2O![]() 4NH3��3O2
4NH3��3O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ������Ԥ����ȷ����
A | B | C | D |
|
|
|
|
�ձ��в�����ɫ������һ��ʱ�����������Ա仯 | ��������ְ�ɫ���ǣ����ȱ���� | KMnO4 ������Һ�ڱ��ͼױ��о���ɫ | Һ��ֲ㣬�²�� ��ɫ |
A.AB.BC.CD.D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����¶ȡ��ݻ���ͬ��3���ܱ������У�����ͬ��ʽͶ�뷴Ӧ����ֺ��¡����ݣ���÷�Ӧ�ﵽƽ��ʱ���й���������[��֪N2��g��+3H2��g��![]() 2NH3��g����H=��92.4kJ/mol]������˵����ȷ���ǣ�������
2NH3��g����H=��92.4kJ/mol]������˵����ȷ���ǣ�������
���� | �� | �� | �� |
��Ӧ��Ͷ���� | 1mol N2��3mol H2 | 2mol NH3 | 4mol NH3 |
NH3��Ũ�ȣ�mol/L�� | c1 | c2 | c3 |
��Ӧ�������仯 | �ų�a kJ | ����b kJ | ����c kJ |
��ϵѹǿ��Pa�� | p1 | p2 | p3 |
��Ӧ��ת���� | ��1 | ��2 | ��3 |
A. 2c1��c3 B. a+b��92.4 C. 2p2��p3 D. ��1+��3��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��---���Ԫ�������ڱ��е�λ����ͼ���Իش��������⣺

��1������Ԫ��������d�����У�________��
��2���ڡ��ۡ�������Ԫ�صĵ�һ�������ɴ�С��˳��Ϊ_________����Ԫ�ط��ű�ʾ����
��3�����Ԫ����Ԫ�����ڱ��е�λ����_______________����ԭ�Ӻ���δ�ɶԵ�����Ϊ_______________�����ԭ�Ӵ��ڻ�̬ʱ��������Ų�ʽΪ___________����֪Ԫ�آ�͢ߵĵ縺�Էֱ�Ϊ1.9��2.5���������γɵĻ���������__________�����������������������������
��4���ۺ�Ԫ��ԭ����ٺ�Ԫ��ԭ���γɵ�ԭ�Ӹ�����Ϊ![]() �ķ���X�ڢ�����γɵĻ�����Y�е��ܽ�Ⱥܴ�����Ҫԭ����____________��
�ķ���X�ڢ�����γɵĻ�����Y�е��ܽ�Ⱥܴ�����Ҫԭ����____________��
��5���ܺź͢ߺ�Ԫ����ɵ�ԭ�Ӹ�����Ϊ3:1��-2�������ӵĿռ乹�͡�����ԭ�ӵ��ӻ����ͷֱ��ǣ�____________��____________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��ʾ�����ӵ�����,������˵������ȷ����
A. 23g ���ڿ����г��ȼ��,ת�Ƶĵ�����ΪNA
B. 50ml 12mol/L��������������MnO2����,��ַ�Ӧ��,ת�Ƶ�����Ϊ0.3NA
C. 0.6mol�������ƾ��������������ӵ���ĿΪ0.6NA
D. ���³�ѹ��,8.8gN2O ��CO2�������������ԭ������Ϊ0.6NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ұ��ҵ�У�����C��Ϊ��ԭ�������¶ȸ���980 Kʱ������������COΪ��������980 Kʱ��CO2Ϊ����
��1����֪2CO(g)![]() CO2(g)��C(s)��T��980 Kʱ��H��T��S��0������ϵ�¶ȵ���980 Kʱ�����Ʀ�H��T��S________0(ѡ����ڡ�����С�ڡ����ڡ�)������ϵ�¶ȸ���980 Kʱ���÷�Ӧ________�Է�����(��ܡ����ܡ�)��
CO2(g)��C(s)��T��980 Kʱ��H��T��S��0������ϵ�¶ȵ���980 Kʱ�����Ʀ�H��T��S________0(ѡ����ڡ�����С�ڡ����ڡ�)������ϵ�¶ȸ���980 Kʱ���÷�Ӧ________�Է�����(��ܡ����ܡ�)��
��2�����ӹ�ҵ����ϴ��Ƭ�ϵ�SiO2(s)�ķ�ӦΪ��
SiO2(s)��4HF(g)===SiF4(g)��2H2O(g)
��H(298.15 K)����94.0 kJ��mol��1
��S(298.15 K)����75.8 J��mol��1��K��1��
�覤H�ͦ�S�����¶ȱ仯���仯����˷�Ӧ�Է����е��¶���________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com