£Ø2011?³ÆŃōĒų¶žÄ££©X”¢Y”¢Z”¢WĖÄÖÖĪļÖŹÓŠČēĻĀĻą»„×Ŗ»Æ¹ŲĻµ£ØĘäÖŠX”¢Wµ„ÖŹ£¬Y”¢ZĪŖ»ÆŗĻĪļ£¬Ī“ĮŠ³ö·“Ó¦Ģõ¼ž£©
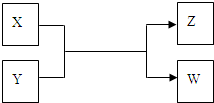
¢ń£®ČōZŹĒÉś»īÖŠ³£ÓƵĵ÷Ī¶Ę·£¬WÓöµķ·ŪČÜŅŗ±äĄ¶£¬Ōņ£ŗ
£Ø1£©³£ĪĀĻĀ£¬XµÄŃÕÉ«ŹĒ
»ĘĀĢÉ«
»ĘĀĢÉ«
£®
£Ø2£©¹¤ŅµÉĻZÓŠ¶ąÖÖÓĆĶ¾£¬ÓĆ»Æѧ·½³ĢŹ½±ķŹ¾ZµÄŅ»ÖÖÓĆĶ¾
2NaCl+2H
2O
H
2ӟ+Cl
2ӟ+2NaOH
2NaCl+2H
2O
H
2ӟ+Cl
2ӟ+2NaOH
£®
£Ø3£©Éś»īÖŠĖłÓƵÄZ¼ÓČėĮĖµāĖį¼Ų£¬¹żĮæXÓėYČÜŅŗ·“Ó¦Ź±æÉŅŌµĆµ½Ņ»ÖÖµāĖįŃĪ£¬“Ė·“Ó¦µÄĄė×Ó·½³ĢŹ½ŹĒ
3Cl2+I-+3H2OØT6Cl-+IO3-+6H+
3Cl2+I-+3H2OØT6Cl-+IO3-+6H+
£®
¢ņ£®ČōXŹĒ¹¤ŅµÉĻÓĆĮæ×ī“óµÄ½šŹōµ„ÖŹ£¬ZŹĒŅ»ÖÖ¾ßÓŠ“ÅŠŌµÄŗŚÉ«¾§Ģ壬Ōņ£ŗ
£Ø1£©XÓėY·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ
£®
£Ø2£©ČōÓĆĻĀĮŠ×°ÖĆÖ»½ųŠŠZ+WØTX+Y·“Ó¦£Ø¼Š³Ö×°ÖĆĪ“»³ö£©£ŗ
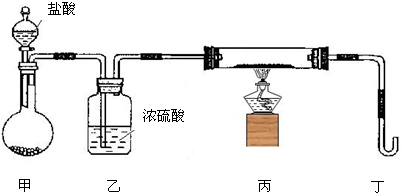
¢ŁĶź³É“ĖŹµŃéÓŠ¶ą²½²Ł×÷£¬ĘäÖŠČż²½ŹĒ£ŗ
a£®µćČ¼¾Ę¾«µĘ
b£®µĪ¼ÓŃĪĖį
c£®¼ģŃéĘųĢå“æ¶Č
ÕāČż²½²Ł×÷µÄĻČŗóĖ³ŠņŹĒ
bca
bca
£ØĢī×ÖÄø£©£®
¢ŚĪŖ±£Ö¤ŹµŃé³É¹¦£¬ÉĻŹö×°ÖĆŠčŅŖøĽų£¬·½·ØŹĒ£ØÓĆĪÄ×ÖŠšŹö£©
ŌŚ¼×”¢ŅŅ×°ÖĆÖŠ¼äŌö¼ÓŅ»øö×°ÓŠĖ®µÄĻ“ĘųĘæ
ŌŚ¼×”¢ŅŅ×°ÖĆÖŠ¼äŌö¼ÓŅ»øö×°ÓŠĖ®µÄĻ“ĘųĘæ
£®
£Ø3£©½«3.48g Z¼ÓČė50mL 4mol/LµÄĻ”HNO
3ÖŠ³ä·Ö·“Ó¦£¬²śÉś112mLµÄNO£Ø±ź×¼×“æö£©£¬Ļņ·“Ó¦ŗóµÄČÜŅŗÖŠµĪ¼ÓNaOHČÜŅŗÄܲśÉś³Įµķ£®µ±³ĮµķĮæ×ī¶ą£¬ÖĮÉŁŠčŅŖ¼ÓČė2mol/LµÄNaOHČÜŅŗ
97.5
97.5
mL £Ø¾«Č·µ½0.1£©£®









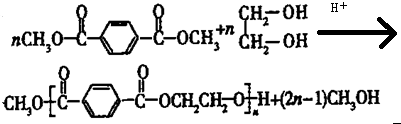
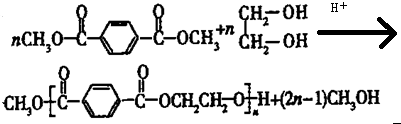
 ŗĻ³É
ŗĻ³É µÄĮ÷³ĢĶ¼£®£Ø×¢Ć÷·“Ó¦Ģõ¼ž£©
µÄĮ÷³ĢĶ¼£®£Ø×¢Ć÷·“Ó¦Ģõ¼ž£©