
相同条件下,0.1mol/L Na2S2O3溶液和0.1mol/L H2SO4溶液各5mL,与10mL水混合,反应时间为t1s;0.2mol/L Na2S2O3溶液和0.2mol/L H2SO4溶液各5mL,与30mL水混合,反应时间为t2 s,则t1和t2的关系是(忽略体积变化)( )
|
| A. | t1>t2 | B. | t1<t2 | C. | t1=t2 | D. | 不能肯定 |
考点:
化学反应速率的影响因素.
专题:
化学反应速率专题.
分析:
对于Na2S2O3溶液和H2SO4溶液的反应来说,如在相同条件下进行,则物质的浓度越大,反应速率越大,可计算各物质的浓度进行比较,以此解答.
解答:
解:0.1mol/L Na2S2O3溶液和0.1mol/L H2SO4溶液各5mL,与10mL水混合,混合后c(Na2S2O3)=c(H2SO4)= =0.025mol/L;
=0.025mol/L;
0.2mol/L Na2S2O3溶液和0.2mol/L H2SO4溶液各5mL,与30mL水混合,混合后c(Na2S2O3)=c(H2SO4)=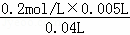 =0.025mol/L,
=0.025mol/L,
两溶液浓度相同,反应速率相同,则t1=t2,
故选C.
点评:
本题考查化学反应速率知识,为高频考点,侧重于学生的分析能力和计算能力的考查,题目从浓度的角度考查化学反应速率的影响,注意把握比较的角度,难度不大.


 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案科目:高中化学 来源: 题型:
乙酰水杨酸即阿斯匹林(aspirin)是一种解热止痛、治疗感冒药,实验室制取原理为:
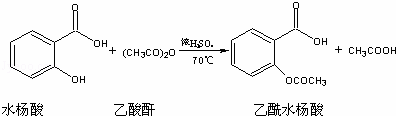
实验方法:在干燥的锥形瓶中放入称量好的水杨酸(6.2g 0.045mol)、乙酸酐(5mL 5.4g 0.053mol),滴入5滴浓硫酸,在70℃反应一段时间,按如下流程分离出乙酰水杨酸.

已知:①乙酰水杨酸溶于热水,在冷水中微溶;乙酸酐遇水生成乙酸.
②乙酰水杨酸钡、水杨酸钡均可溶于水.
(1)反应后用40mL冰水稀释反应混合物的操作是: .
(2)操作Ⅰ为 .
(3)判断粗产物与饱和碳酸氢钠反应完全的现象是: .
(4)某同学推测产品中可能还含有少量水杨酸和Na2SO4,设计了如下方案进行检验,实验证明不含杂质,请在答题卡上完成表中内容.
序号 实验方案 实验现象 结论
① 将少量产品加入6mL水的试管A中,振荡,将上层液体倾析至B、C中. 得到白色晶体和无色溶液
② 产品中不含Na2SO4
③ 向试管C中,加入少量FeCl3溶液(或浓溴水). 溶液不显紫色(或无白色沉淀出现). 产品中不含水杨酸
(5)产率计算:称量干燥后纯净产品质量为3.2g,该实验中乙酰水杨酸的产率计算表达式为×100%,计算结果为40%(保留两位有效数字).(乙酰水杨酸的相对分子质量为180)
查看答案和解析>>
科目:高中化学 来源: 题型:
含等物质的量NaOH的溶液分别用pH为2和3的CH3COOH溶液中和,设消耗CH3COOH溶液的体积依次为Va、Vb,则两者的关系正确的是( )
|
| A. | Va>10Vb | B. | Va=10Vb | C. | Vb<10Va | D. | Vb>10Va |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子:(1)I﹣、Fe2+、NO3﹣、H+(2)K+、NH4+、HCO3﹣、OH﹣ (3)SO32﹣、SO42﹣、K+、OH﹣(4)Fe2+、Cu2+、SO42﹣、Cl﹣ (5)Fe3+、SCN﹣、K+、SO42﹣ (6)H+、K+、AlO2﹣、HSO3﹣ 在溶液中能大量共存且溶液为无色的组别共有( )
|
| A. | 1组 | B. | 2组 | C. | 3组 | D. | 不少于4组 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图为某化学反应的速率与时间的关系示意图.在t1时刻升高温度或增大压强,速率的变化都符合示意图的反应是( )
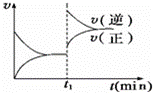
|
| A. | 2SO2(g)+O2(g)⇌2SO3(g);△H<0 |
|
| B. | 4NH3(g)+5O2(g)⇌4NO(g)+6H2O(g);△H<0 |
|
| C. | H2(g)+I2(g)⇌2HI(g);△H>0 |
|
| D. | C(s)+H2O(g)⇌CO(g)+H2(g);△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
以下框图中A~M是中学化学常见的物质,其中A、E是金属,F和J为气体单质,其余均为化合物或其溶液,C为淡黄色固体,D为红棕色粉末,M为红褐色固体.

(1)B的化学式 ;
(2)19.5gC与足量的水反应转移电子的物质的量为 mol;
(3)写出物质C的电子式 ;
(4)写出②、③反应的方程式② ,③ .
查看答案和解析>>
科目:高中化学 来源: 题型:
在元素周期表中位于金属元素和非金属元素交界处最容易找到的材料是()
A. 制催化剂的材料 B. 半导体材料
C. 制农药的材料 D. 耐高温、耐腐蚀的合金材料
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素A、B、C、D、E的原子序数依次增大,其中B和E同主族.A元素的最高正化合价和最低负化合价的绝对值之差为2;1mol C单质与冷水反应,在标准状况下生成11.2L H2;D原子最外层电子数等于其周期序数;E﹣的电子层结构与Ar原子相同.
(1)用元素符号表示各元素A 、B 、C 、D 、E ;
(2)能形成共价键的元素
(3)A的单质的电子式为
(4)C和B形成化合物的电子式
(5)写出C与水反应的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒容密闭容器中通入X并发生反应:2X(g)⇌Y(g),温度T1、T2下X的物质的量浓度c(X)随时间t变化的曲线如图所示.下列叙述正确的是()

A. 该反应进行到M点放出的热量大于进行到W点放出的热量
B. T2下,在0~t1时间内,v(Y)=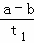 mol•L﹣1•min﹣1
mol•L﹣1•min﹣1
C. M点的正反应速率V正大于N点的逆反应速率V逆
D. M点时再加入一定量X,平衡后X的转化率减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com