
体积为1ml、浓度均为0.10mol/L的XOH和X2CO3溶液,分别加水稀释至体积V,pH随lgV的变化情况如图所示,下列叙述中正确的是
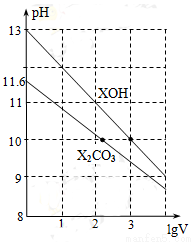
A.XOH是弱碱
B.pH=10的两种溶液中的c(X+):XOH大于X2CO3
C.已知H2CO3的电离平衡常数Ka1远远大于Ka2,则Ka2约为1.0×10-10.2
D.当lgV=2时,若X2CO3溶液升高温度,溶液碱性增强,则c(HCO3-)/c(CO32-)减小
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案科目:高中化学 来源:2016-2017学年宁夏高二上期中化学卷(解析版) 题型:推断题
软质隐形眼镜材料W、树脂X的合成路线如图所示。

(1)A中含有的官能团的结构简式是_______________。
(2)甲的结构简式是_______________。
(3)B→C反应的化学方程式是____________________________。
(4)B有多种同分异构体.属于酯且含有碳碳双键的同分异构体共有______________种(不考虑顺反异构。
(5)已知F的相对分子质量为110,1molF可与足量钠反应生成22.4L氢气(标准状况下),
苯环上的氢原子化学环境都相同.则F还能发生的反应是 _______________(填序号)
_______________(填序号)
a.加成反应 b.氧化反应 c.加聚反应 d.水解反应
(6)写出树脂X可能的结构简式_______________(写出一种即可)。
(7)E的分子式为C10H14O2,含三个甲基,苯环上的一溴代物有两种,生成E的化学方程式是________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高二上月考二化学卷(解析版) 题型:填空题
电化学综合应用
(Ⅰ) 选择合适的图象:

(1)将等质量的两份锌粉a、b分别加入过量的稀硫酸中,同时向a中加入少量的CuSO4溶液,产生H2的体积V(L)与时间t(min)的关系是_____________。
(2)将(1)中的CuSO4溶液改成CH3COONa溶液,其他条件不变,则图象是 。
(Ⅱ)如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:

(1)甲烷燃料电池负极反应式是_________________________。
(2)乙装置中铁极的电极反应式为_______________________。
(3)检验石墨(C)极反应产物的方法是____________ _________。
(4)若在标准状况下,有2.24 L氧气参加反应,丙装置中阴极析出铜的质量为________g。

(Ⅲ)Na2FeO4是一种既能杀菌、消毒,又能絮凝净水的高效水处理剂,其电解制法如图所示。电解过程中,两极均有气体产生,Y极区域溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍澄清。查阅资料得知,高铁酸根离子(FeO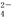 )在溶液中呈紫红色。
)在溶液中呈紫红色。
(1)电解过程中,X极区溶液的pH___________(填“增大”“减小”或“不变”)。
(2)电解过程中,Y极发生的电极反应为Fe-6e-+8OH-===FeO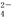 +4H2O和_____ _____。
+4H2O和_____ _____。
(3)若在X极收集到672 mL气体,在Y极收集到168 mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少__________g。
(4)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为2K2FeO4+3Zn===Fe2O3+ZnO+2K2ZnO2。该电池正极发生的反应的电极反应式为____________________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高二上月考二化学卷(解析版) 题型:选择题
酚酞是中学阶段常用的酸碱指示剂,已知的结构简式如图所示:下列关于酚酞的说法正确的是

A.酚酞属于芳香烃
B.酚酞的分子式为C20H12O4
C.酚酞结构中含有羟基(—OH),故酚酞属于醇
D.酚酞在碱性条件下能够发生水解反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上期中化学卷(解析版) 题型:选择题
t℃时,某平衡体系中含有X、Y、Z、W四种物质,此温度下发生反应的平衡常数表达式为:  。有关该平衡体系的说法正确的是
。有关该平衡体系的说法正确的是
A.升高温度.平衡常数K一定增大
B.增大压强.W(g)质量分数增加
C.升高温度.若混合气体的平均相对分子质量变小.则正反应是放热反应
D.增大X(g)浓度.平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上期中化学卷(解析版) 题型:选择题
下列叙述错误的是
A.生铁中含有碳,抗腐蚀能力比纯铁弱
B.用锡焊接的铁质器件,焊接处易生锈
C.铁管上镶嵌锌块,铁管不易被腐蚀
D.在铁制品上镀铜时,镀件为阳极,铜盐为电镀液
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上期中化学卷(解析版) 题型:选择题
下列表述中正确的是
A.任何能使熵值增大的过程都自发进行
B.已知热化学方程式2SO2(g)+O2(g)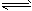 2SO3(g) ΔH=-Q kJ·mol-1(Q>0),则将2mol SO2(g)和1mol O2(g)置于一密闭容器中充分反应后放出Q kJ的热量
2SO3(g) ΔH=-Q kJ·mol-1(Q>0),则将2mol SO2(g)和1mol O2(g)置于一密闭容器中充分反应后放出Q kJ的热量
C.人类利用的能源都是通过化学反应获得的
D.1 mol NaOH分别和1 mol CH3COOH、1 mol HNO3反应,后者比前者放出的热量多
查看答案和解析>>
科目:高中化学 来源:2017届山东省泰安市高三上学期期中化学试卷(解析版) 题型:选择题
用含少量镁粉的铝粉制取纯净的氢氧化铝,下述操作步骤中最恰当的组合是
①加盐酸溶解 ②加烧碱溶液溶解 ③过滤 ④通入过量 CO2生成Al(OH)3沉淀
CO2生成Al(OH)3沉淀
⑤加入盐酸,生成Al(OH)3沉淀⑥加入过量烧碱溶液
A.①⑥⑤③ B.②③④③
C.②③⑤③ D.①③⑤③
查看答案和解析>>
科目:高中化学 来源:2017届辽宁省高三第三次月考化学试卷(解析版) 题型:选择题
在体积不变的400℃恒温密闭容器中,一定量的SO2与1mol O2在催化剂作用下发生反应:2SO2(g)+O2(g)  2SO3(g) ΔH =-Q kJ ∕ mol(Q﹥0)。当气体的物质的量减少0.5 mol时反应达到平衡。下列叙述错误的是( )
2SO3(g) ΔH =-Q kJ ∕ mol(Q﹥0)。当气体的物质的量减少0.5 mol时反应达到平衡。下列叙述错误的是( )
A.增大氧气浓度,平衡正向移动,平衡常数不变
B.降低温度,正反应速率比逆反应速率减小的程度小
C.平衡时SO2气体的转化率为50%
D.该条件下反应放出0.5Q kJ的热量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com