
| A. | 橙色变为黄色 | B. | 黄色变为橙色 | C. | 橙色变为红色 | D. | 红色变为橙色 |
分析 甲基橙的变色范围为3.1~4.4,pH小于3.1显示红色、大于4.4显示黄色、3.1~4.4之间显示橙色,待测液是氢氧化钠,滴入甲基橙后溶液颜色是黄色,根据以上分析进行判断.
解答 解:甲基橙的变色范围为3.1~4.4,pH小于3.1显示红色、大于4.4显示黄色、3.1~4.4之间显示橙色,
待测液是氢氧化钠,锥形瓶中盛有的氢氧化钠溶液中滴入甲基橙,溶液的颜色是黄色,随着溶液的pH减小,当滴到溶液的pH小于4.4时,溶液颜色由黄色变成橙色,且半分钟不褪色,滴到结束,
所以滴定终点时的颜色变化为:黄色变成橙色,
故选B.
点评 本题考查了中和滴定,题目难度不大,明确甲基橙不是范围为解答关键,注意掌握判断中和滴定的滴定终点的判断方法,试题培养了学生的分析能力及灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 14C与14N互为同位素 | B. | 淀粉和纤维素互为同分异构体 | ||
| C. | CH4与(CH3)2CHCH3互为同系物 | D. | H2O与D2O互为同素异形体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 已知:H2S在高温下分解生成硫蒸气和H2.现测得某温度下,H2S分解过程中各物质的物质的量随时间变化关系如图所示,则生成的硫蒸气化学式为( )
已知:H2S在高温下分解生成硫蒸气和H2.现测得某温度下,H2S分解过程中各物质的物质的量随时间变化关系如图所示,则生成的硫蒸气化学式为( )| A. | S | B. | S2 | C. | S6 | D. | S8 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2分子的空间构型为直线形 | |
| B. | CO2分子为非极性分子 | |
| C. | BF3分子中的B原子满足8电子稳定结构 | |
| D. | CH3COOH分子中C原子均为sp3杂化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
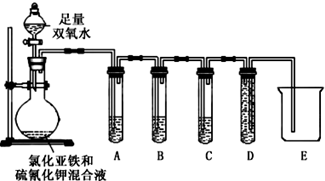
| 实验过程和现象 | 结论 |
| (2)试管A中盛有品红溶液现象:品红溶液褪色 | 证明气体中含有SO2 |
| (3)试管B中现象紫色酸性高锰酸钾溶液颜色不变或变浅试管C中现象:澄清石灰水变浑浊 | 证明气体中含有CO2 |
| 实验过程 | 实验现象及结论 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ③>②>① | B. | ②>①>③ | C. | ①>②>③ | D. | ②>③>① |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com